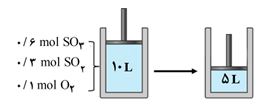
تعادل $2S{O_2}(g) + {O_2}(g) \rightleftharpoons 2S{O_3}(g) + Q$ در سیلندری مجهز به پیستون روان در دمای ثابت برقرار است.
الف) ثابت تعادل واکنش را محاسبه کنید.
ب) اگر حجم پیستون به 5 لیتر کاهش یابد، شمار مولکولهای اکسیژن چه تغییری میکند؟ چرا؟
ج) برای افزایش میزان پیشرفت واکنش، افزایش دما مناسبتر است یا کاهش دما؟