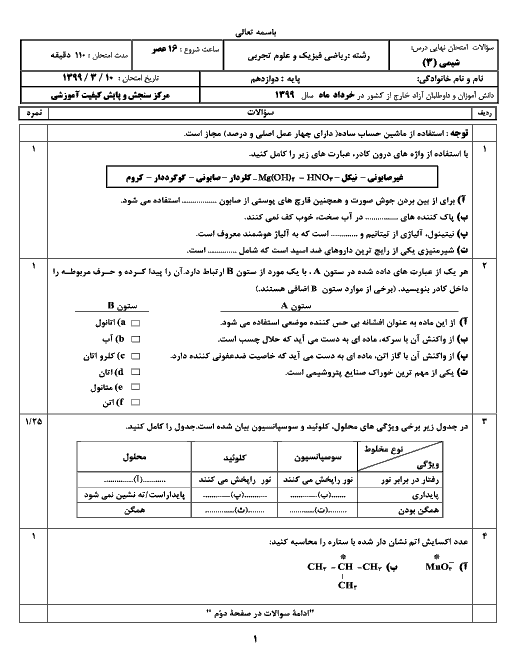
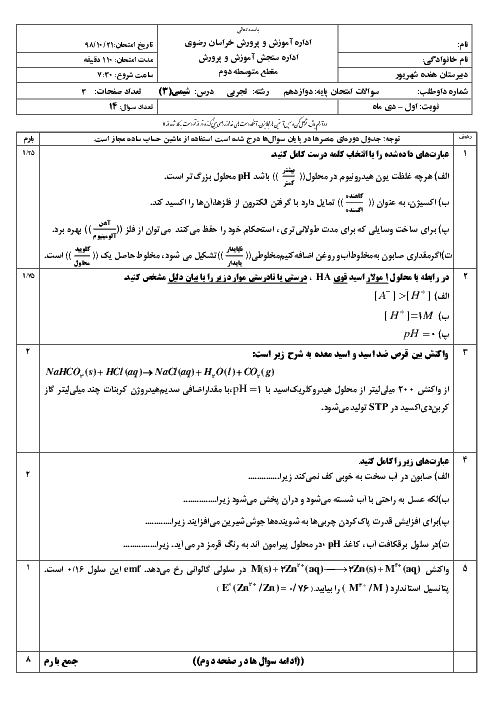
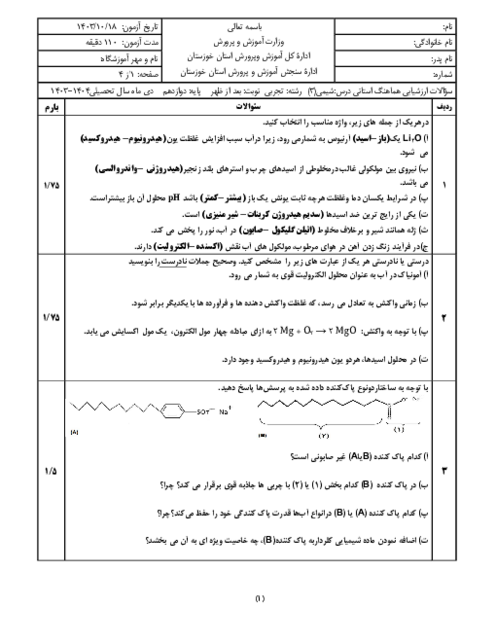
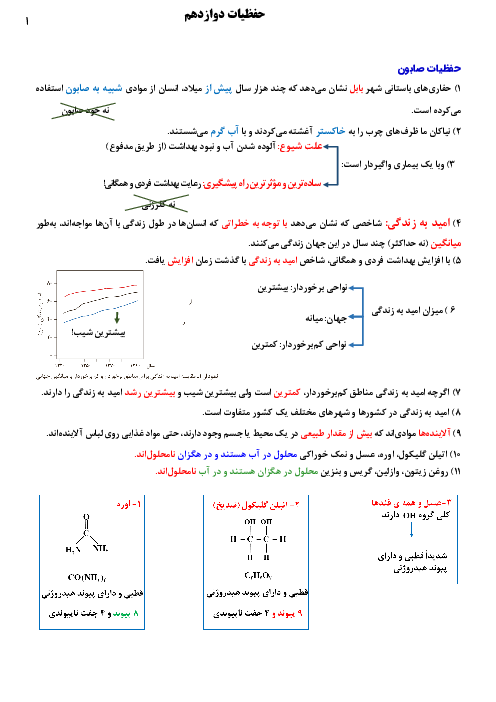
$pH$ محلول $0/001$ مولار هيدروفلوئوريکاسيد، با $pH$ محلول اسید $HX$ که غلظت یون ${{H}_{3}}{{O}^{+}}$ در محلول آن ${{10}^{-3/7}}$ مول بر ليتر میباشد، برابر است. مقدار ثابت يونش هيدروفلوئوريک اسيد كدام است؟
1 )
$3\times {{10}^{-6}}$
2 )
$4\times {{10}^{-5}}$
3 )
$3\times {{10}^{-5}}$
$5\times {{10}^{-5}}$