چند مورد از موارد زیر صحیحاند؟
$\bullet $ با اعمال هرگونه تغییر که سبب برهم خوردن یک سامانه تعادلی شود، واکنش تا زمانی در یکی از جهتها جابهجا میشود که به تعادل جدید برسد.
$\bullet $ در سامانۀ تعادلی ${{H}_{2}}(g)+{{I}_{2}}(g)\rightleftharpoons 2HI(g)$ اعمال هرگونه تغییری سبب برهم خوردن تعادل و جابهجایی آن میشود.
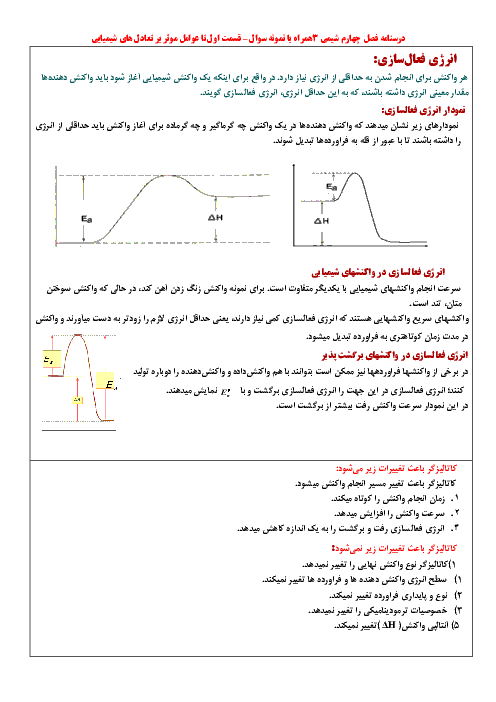
$\bullet $ در تولید آمونیاک به روش هابر، برای رفع مشکل عامل دما، از کاتالیزگر استفاده میشود.
$\bullet $ در تعادلهای گرماده، دما رابطۀ معکوس با مقدار عددی K و غلظت فراوردههای گازی و محلول دارد.
$\bullet $ در تعادل ${{N}_{2}}(g)+3{{H}_{2}}(g)\rightleftharpoons 2N{{H}_{3}}(g)$ ، برای جدا کردن $N{{H}_{3}}$ از مخلوط تعالی، میتوان ظرف را در دمای $-{{50}^{\circ }}C$ قرار دارد.