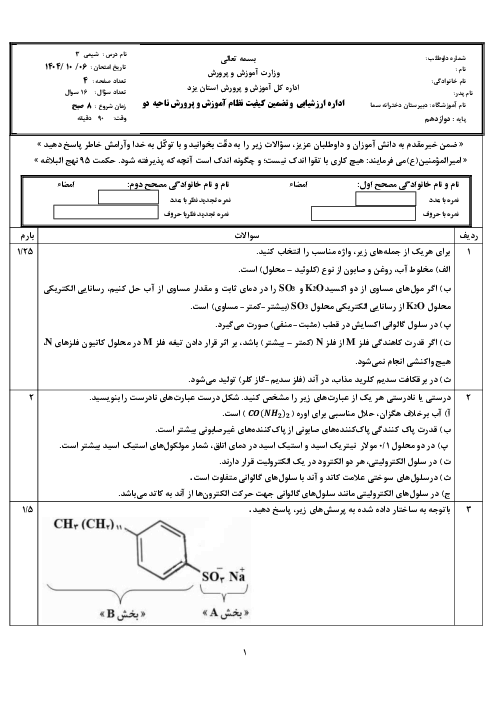
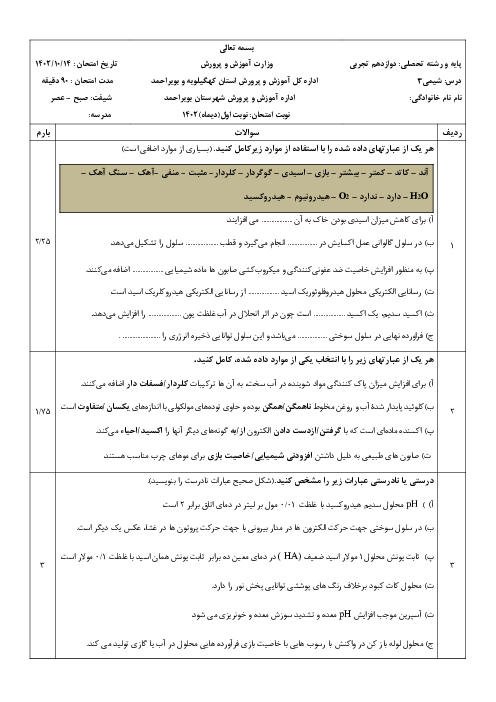
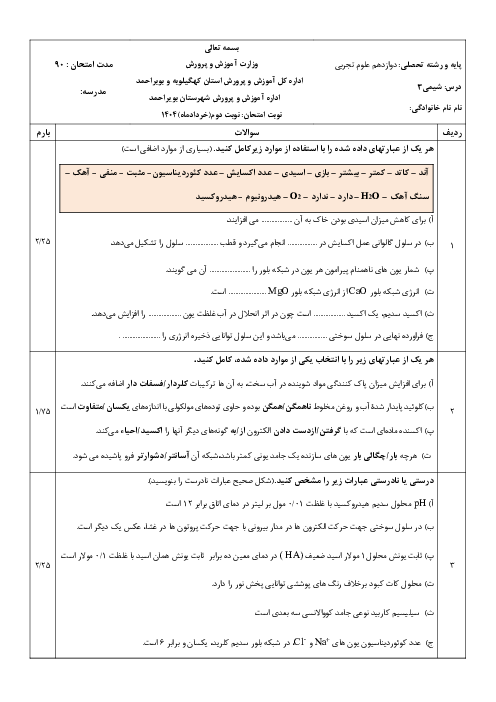
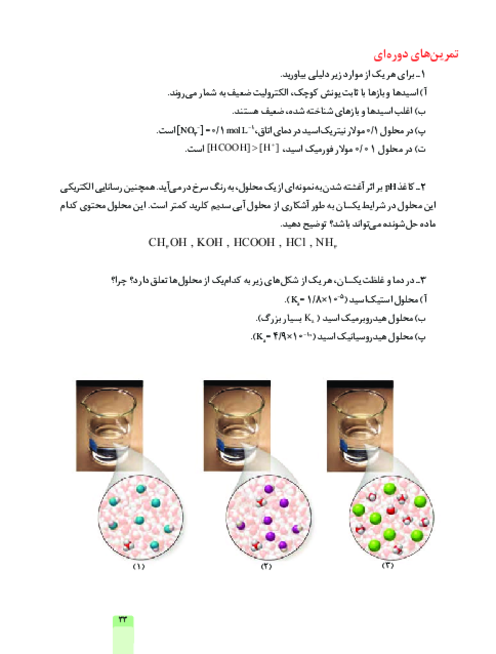
قسمت 3: اسیدها و بازها و رسانایی الکتریکی و درجه یونش اسیدها
شیمی (3)
دوازدهم
متوسطه دوم نظری
علوم ریاضی
درسنامه آموزشی این مبحث
اگر درصد یونش در محلولی از استیک اسید $(C{H_3}COOH)$ برابر با 3/2% و غلظت یون هیدرونیوم در آن $1/92 \times {10^{ - 2}}$ مول بر لیتر باشد.
الف) معادله یونش این اسید را بنویسید.
ب) غلظت محلول را محاسبه کنید.