درحال دریافت اطلاعات ...
{{ title }} با پاسخ {{ subtitle }}
-
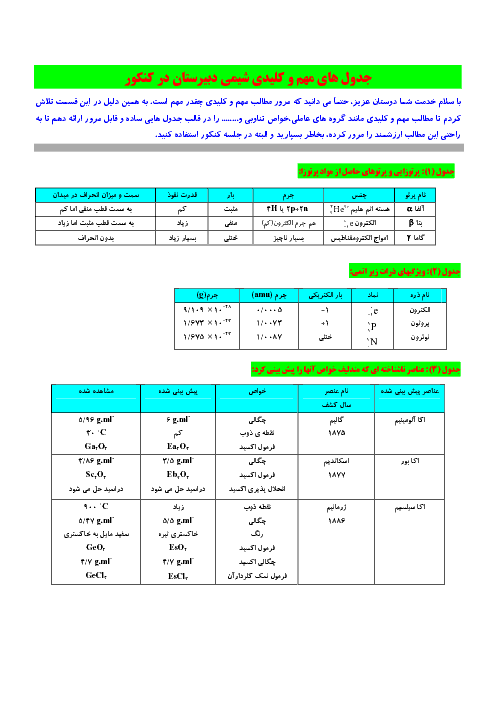
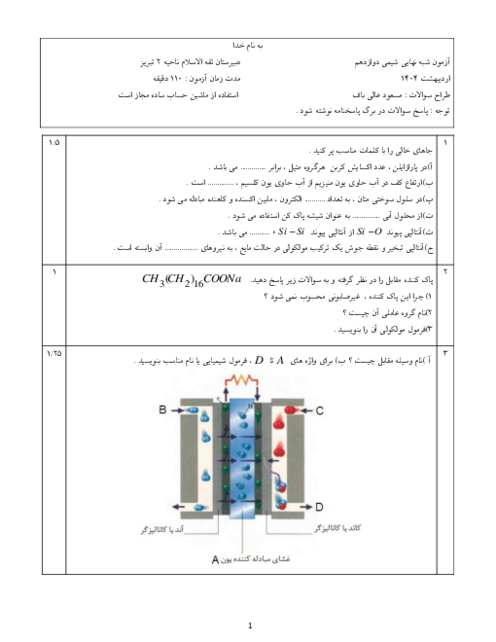
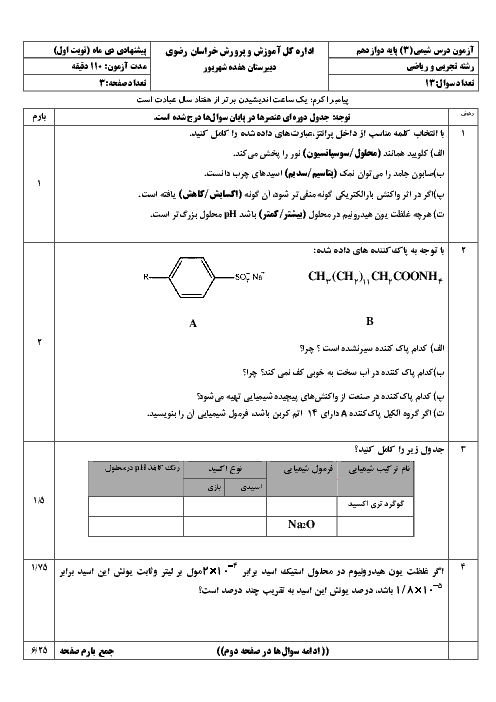
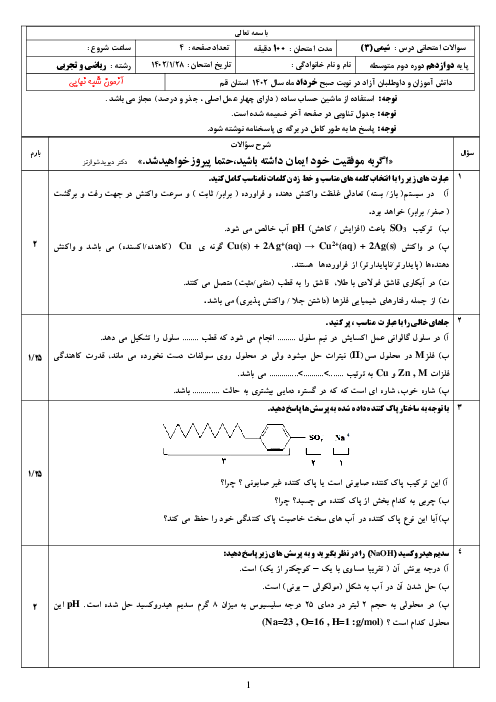
شیمی (3)
- فصل 1: مولکولها در خدمت تندرستی
- فصل 2: آسایش و رفاه در سایه شیمی
- فصل 3: شیمی جلوهای از هنر، زیبایی و ماندگاری
- فصل 4: شیمی، راهی به سوی آیندهای روشنتر