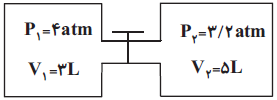
مطابق شكل، دو گاز آرمانی در دماي يکسان، داخل دو مخزن هستند. اگر شير رابط بين دو مخزن را باز كنيم تا گازها در دمای ثابت اوليه به تعادل برسند، فشار مخازن پس از تعادل، برحسب اتمسفر كدام است؟

گاما رو نصب کن!
جستجو
پربازدیدها: #{{ tag.title }}
به پاس اعتمادی که به گاما داشتی، ما اشتراک ویژهای رو برات فعال کردیم تا بدون هیچ نگرانی از محدودیت زمانی، از سرویسهای ویژه گاما استفاده کنی.
اگه به اطلاعات بیشتری نیاز داری راهنمای تغییرات جدید رو ببین.
از همراهیت با گاما سپاسگزاریم.
با تقدیم احترام
با سپاس! گزارش شما ثبت شد.
مطابق شكل، دو گاز آرمانی در دماي يکسان، داخل دو مخزن هستند. اگر شير رابط بين دو مخزن را باز كنيم تا گازها در دمای ثابت اوليه به تعادل برسند، فشار مخازن پس از تعادل، برحسب اتمسفر كدام است؟
