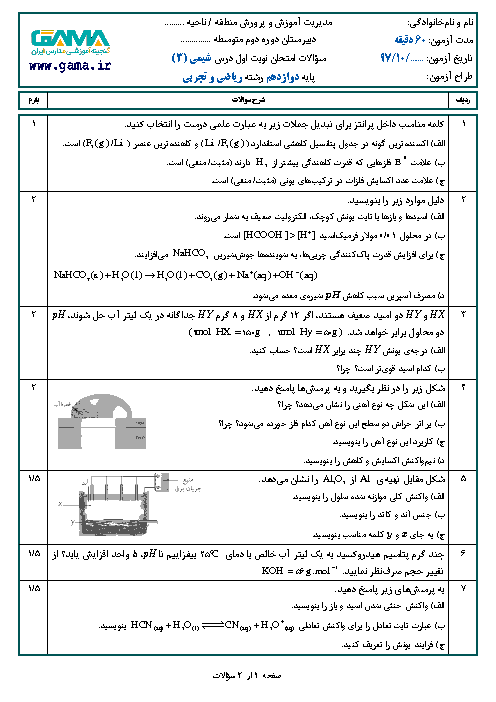
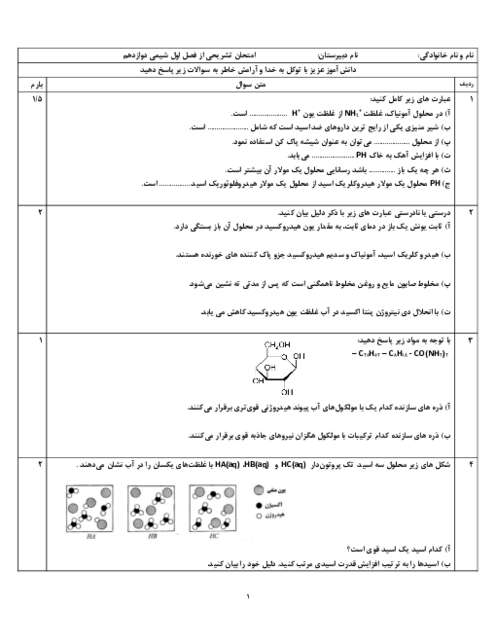
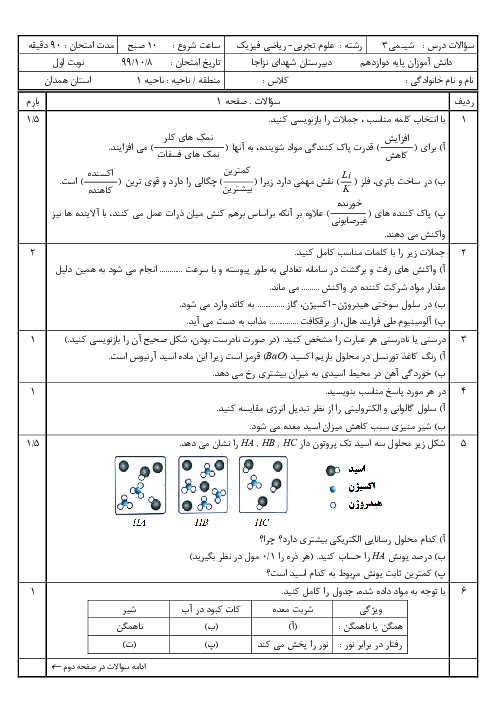
با توجه به جدول زیر که اثر دما را بر ثابت تعادل واکنش «${N_2}(g) + 3{H_2}(g) \rightleftarrows 2N{H_3}(g):\Delta H \lt 0 $» نشان میدهد، به پرسش ها پاسخ دهید:
الف) عبارت ثابت تعادل را برای این واکنش بنویسید.
ب) میزان پیشرفت این واکنش در کدام دما بیشتر است؟ چرا؟
پ) با افزایش دما K که تغییری کرده است؟ دلیل خود را به کمک اصل لوشاتیله توجیه کنید.

پاسخ تشریحی :
تحلیل ویدئویی تست
منتظریم اولین نفر تحلیلش کنه!