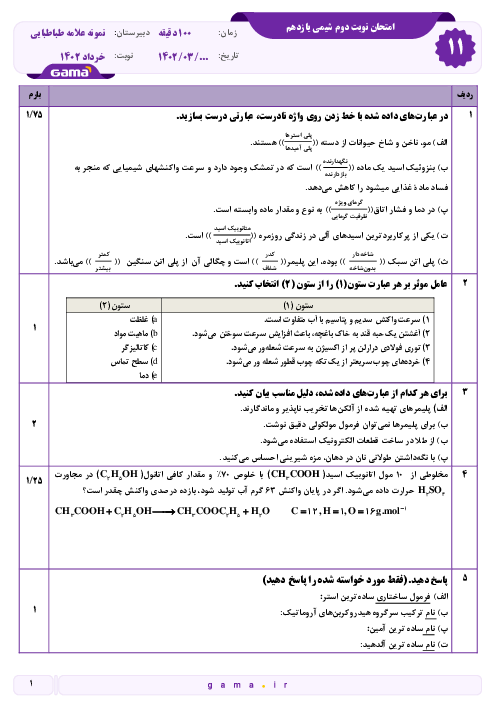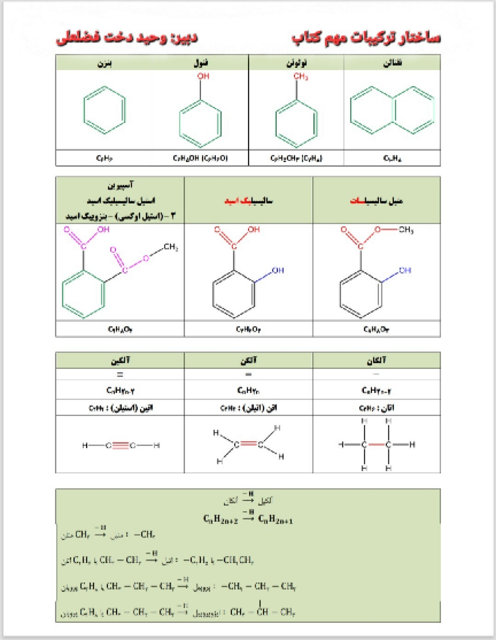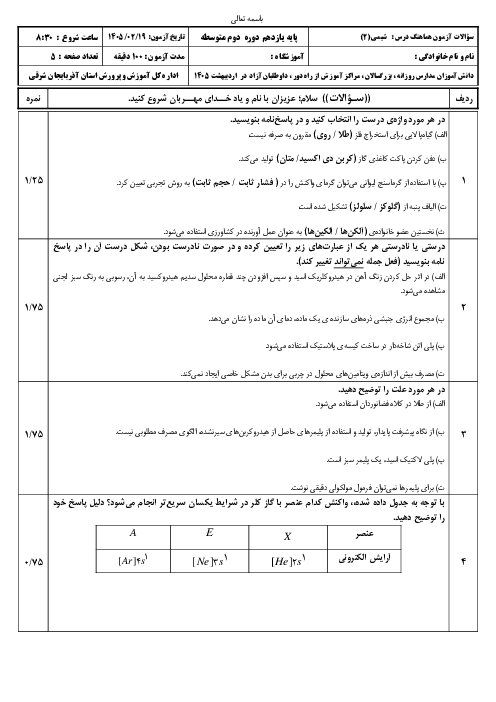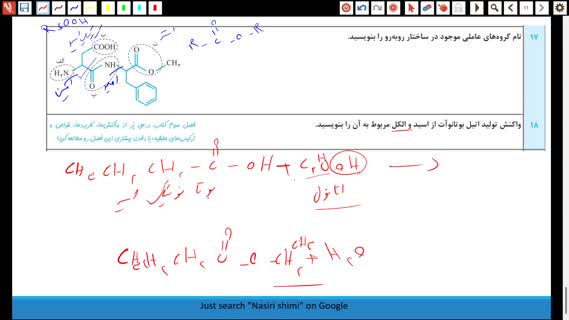
قسمت 1 - صفحه 1 تا 121 - حل نمونه سوال استاندارد امتحان ترم دوم شیمی یازدهم

قسمت 2 - صفحه 72 تا 75 - قانون هس | حل سوالات تستی شیمی یازدهم
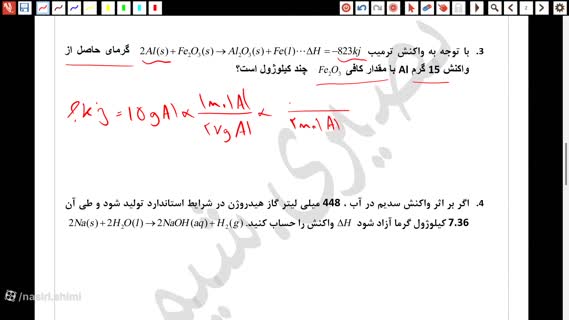
قسمت 3 - صفحه 72 تا 75 - فیلم آموزش حل مسائل استوکیومتری آنتالپی | شیمی یازدهم فصل دوم
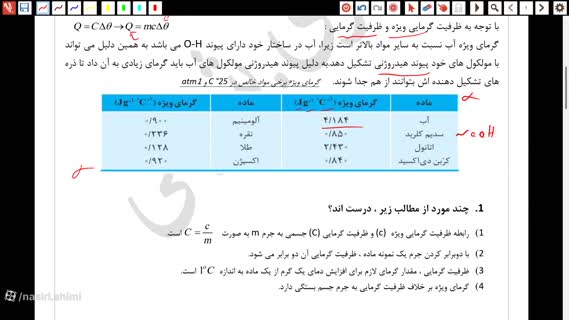
قسمت 4 - صفحه 72 تا 75 - فیلم آموزش حل مسائل ظرفیت گرمایی و گرمای ویژه | شیمی یازدهم فصل دوم

شمار واحدهای گلوکز در پلیمرهای طبیعی و ساختگی

ارتباط سرعت واکنش با ضریب استوکیومتری

حل نمونه سوال محاسبه ارزش سوختی با استفاده از آنتالپی

حل نمونه سوال آنتالپی سوختن
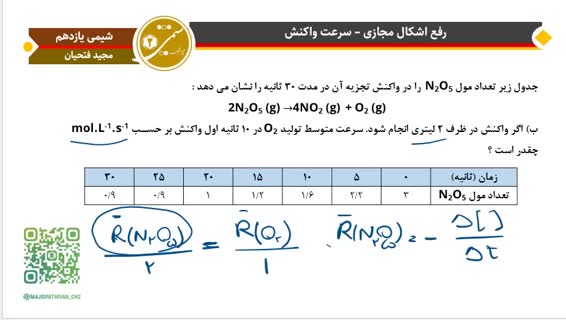
حل نمونه سوال سرعت متوسط مصرف واکنش دهنده و تولید فرآورده

حل سؤالات شیمی یازدهم در کنکور سراسری تیر ماه 1404 رشته تجربی

فیلم حل نمونه سوال سرعت واکنش

حل سؤالات شیمی یازدهم در کنکور سراسری تیر ماه 1404 رشته ریاضی

بررسی و حل سؤالات شیمی یازدهم نهایی خرداد 1404

فیلم حل نمونه سوال شیمی یازدهم | آنتالپی واکنش
موارد مشابه بیشتر
حل مسائل آنتالپی واکنشها با قانون هس
باز نشر محتواها در فضای مجازی، ممنوع است.