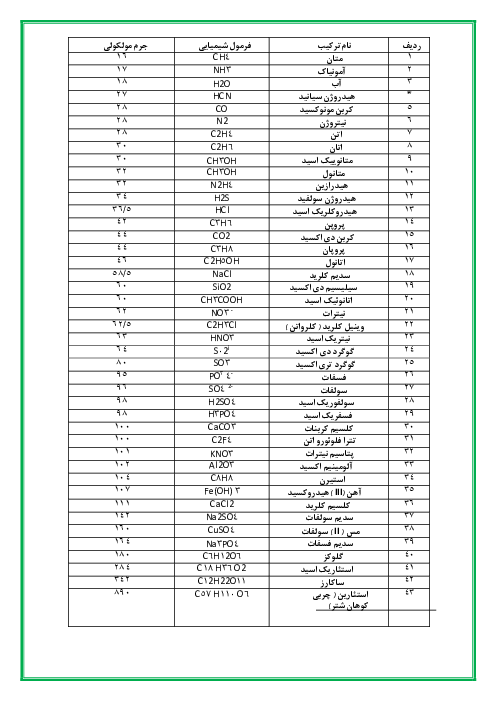
کدام مورد درست است؟ $(H = 1,C = 12,O = 16:g.mo{l^{ - 1}})$
1 )
براساس مدل آرنیوس، در دما و غلظت یکسان، محلول HF، اسیدیتر از محلول HCN است.
2 )
اگر غلظت آنیون، در محلول اسید قوی HA، و محلول اسید ضعیف HX، برابر باشد، غلظت مولکولهای آغازی حل شده نیز برابر است.
3 )
هرچه $\left[ {{H^ + }} \right]$ در محلول باز قوی بیشتر باشد، pH آن بزرگتر و هرچه $\left[ {O{H^ - }} \right]$ در محلول اسید قوی کمتر باشد، pH آن کوچکتر است.
اگر در دمای ثابت و در دو ظرف جداگانه با حجم یکسان، جرم فرمیک اسید حل شده، 0/92 برابر جرم استیکاسید حل شده باشد، شمار یونها در محلول فرمیکاسید بیشتر است.
تحلیل ویدئویی تست
منتظریم اولین نفر تحلیلش کنه!