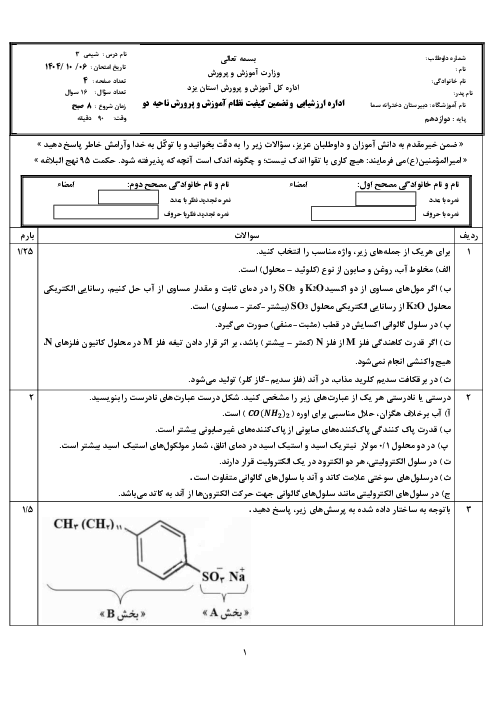
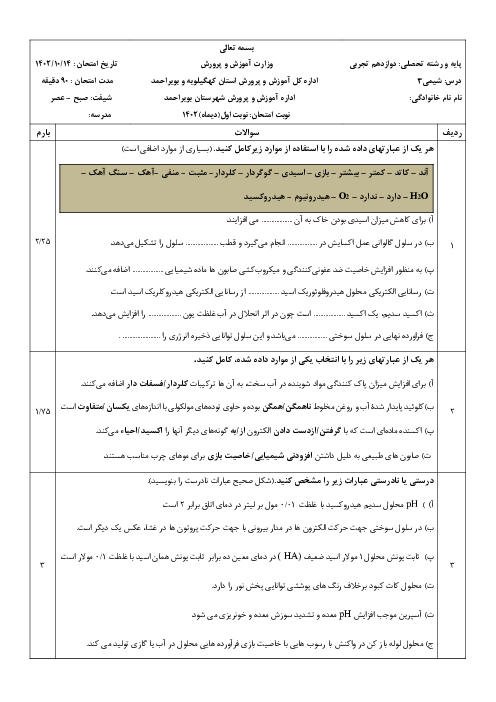
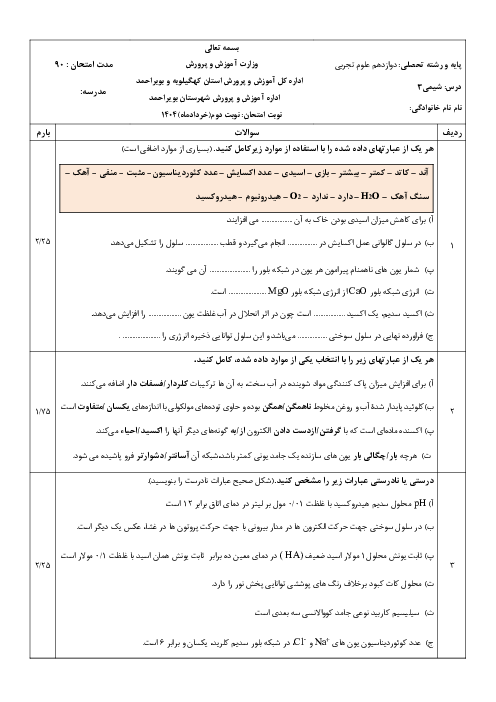
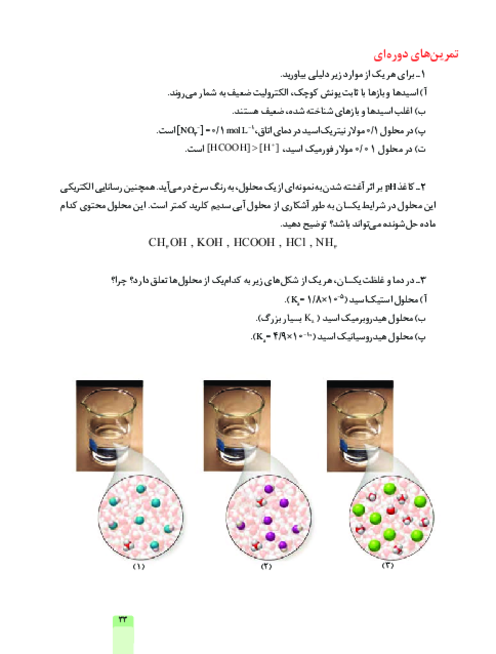
$\begin{aligned} & H F \underset{\leftarrow}{\rightarrow} H^{+}+F^{-} \Rightarrow\left[O H^{-}\right]=10^{-10 / 3} \\ & \Rightarrow\left[O H^{-}\right] \times\left[H^{+}\right]=10^{-14} \Rightarrow\left[H^{+}\right]=\frac{10^{-14}}{10^{-10 / 3}}=10^{-3 / 7} \\ & \Rightarrow \log 2=0,3 \Rightarrow 10^{-3 / 7}=10^{-4} \times 10^{0 / 3}=2 \times 10^{-4} \\ & =2 / 5 \times 10^{-2} \\ & =2 / 5 \Rightarrow a\end{aligned}$
$$
\begin{aligned}
& \Rightarrow a=\frac{\left[\mathrm{H}^{+}\right]}{M} \Rightarrow M=\frac{\left[\mathrm{H}^{+}\right]}{a}=\frac{2 \times 10^{-4}}{2 / 5 \times 10^{-2}}=8 \times 10^{-3} \frac{\mathrm{~mol}}{\mathrm{Lit}} \\
& =8 \times 10^{-3} \times 100=8 \times 10^{-1}
\end{aligned}
$$
$$
\Rightarrow M=\frac{\operatorname{mol} H F}{V_{\mathrm{JA}}} \Rightarrow H F
$$