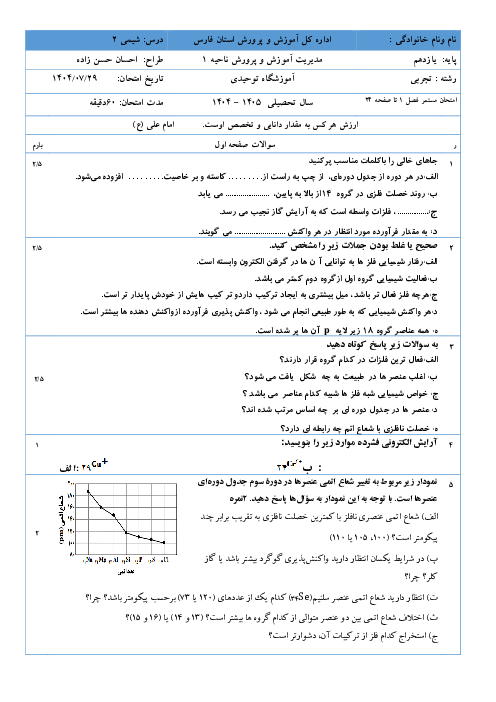
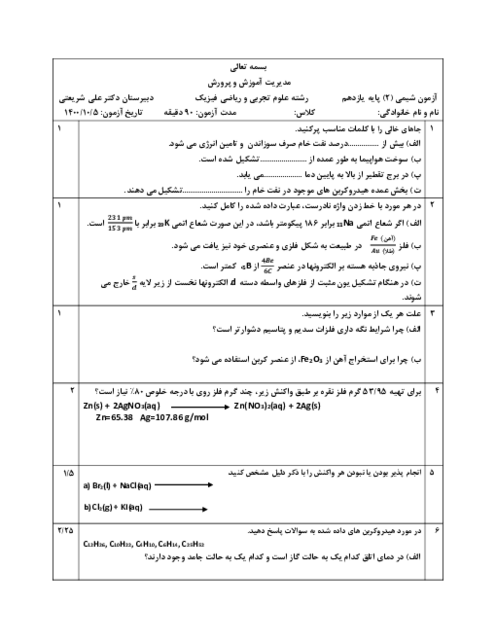
اگر در آغاز واکنش $3 A(g)+4 B(g) \rightarrow 2 C(g)+D(g)$، مجموع شمار مولهای گازی موجود در ظرف 5 لیتری واکنش، 2/8 مول باشد و پس از گذشت 2 دقیقه این مقدار به 2/4 مول کاهش یابد، سرعت متوسط واکنش در این بازه زمانی کدام است؟ (در ابتدای واکنش، فقط واکنشدهندهها حضور دارند.)
$0 / 01 \mathrm{~mol} \cdot \mathrm{~L}^{-1} \cdot \mathrm{~min}^{-1}$
2 )
$0 / 2 \mathrm{~mol} \cdot L^{-1} \cdot \mathrm{~s}^{-1}$
3 )
$0 / 02 \mathrm{~mol} \cdot \mathrm{~L}^{-1} \cdot \mathrm{~min}^{-1}$
4 )
$0 / 1 \mathrm{~mol} \cdot L^{-1} \cdot \mathrm{~s}^{-1}$
پاسخ تشریحی :
تحلیل ویدئویی تست
منتظریم اولین نفر تحلیلش کنه!