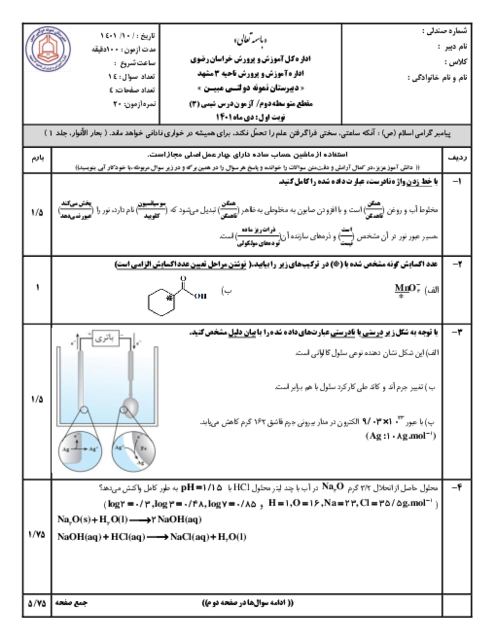
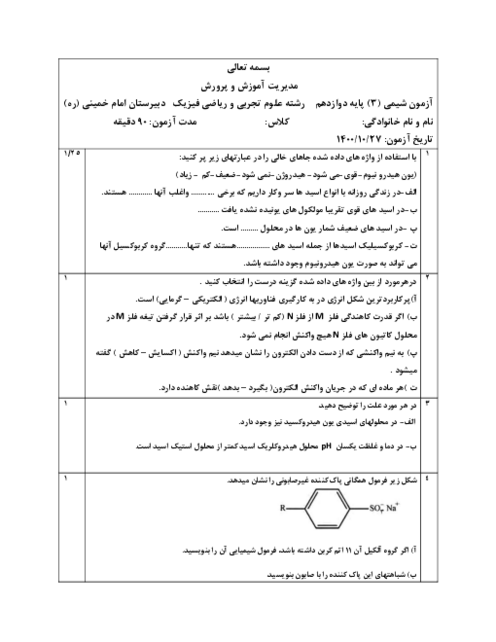
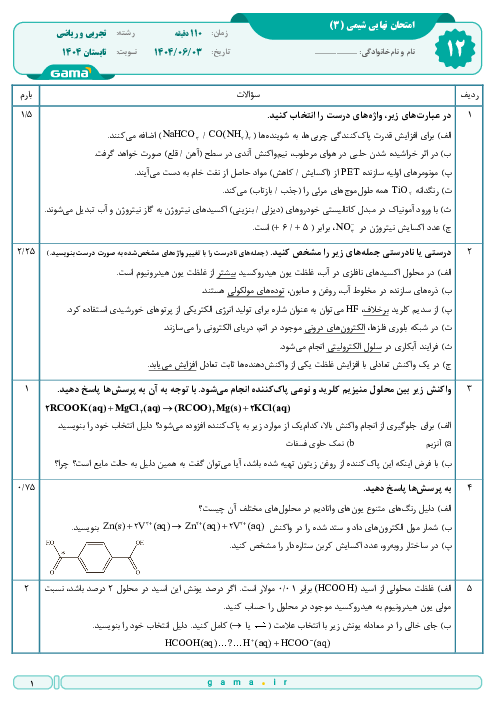
همانطور که میدانید، معده برای گوارش غذا به اسید نیاز دارد. خوردن غذا باعث میشود که غدههای موجود در دیوارهی معده، هیدرولیک اسید $(HCl)$ ترشح کنند.
در بدن انسان بالغ روزانه بین $2$ تا $3$ لیتر شیرهی معده، تولید میشود که غلظت یون هیدرونیوم در آن حدود $0/03mol{{L}^{-1}}$ است؛ یعنی $PH$ شیرهی معده حدود $1/5$ میباشد.
$\left[ {{H}^{+}} \right]=\left[ HCl \right]=0/03mol{{L}^{-1}}\Rightarrow PH=-\log \left[ {{H}^{+}} \right]=-\log 0/03=-\log (3\times {{10}^{2}})=2-\log 3=2-0/5=1/5$
پس درون معده یک محیط بسیار اسیدی است، به طوریکه میتواند فلز روی $(Zn)$ را در خود حل کند.
\[Zn(s)+2HCl(aq)\to ZnC{{l}_{2}}(aq)+{{H}_{2}}(g)\]
دیوارهی داخلی معده هم به طور طبیعی مقدار کمی از یونهای هیدرونیوم را جذب میکند که متأسفانه! باعث نابودی سلولهای سازندهی دیوارهی معده میشود (در این شرایط در هر دقیقه حدود $0/5$ میلیون سلول از بین میرود). حالا اگر مقدار اسید معده به هر دلیل بیش از ادازه باشد، شمار یونهای ${{H}^{+}}$ جذب شده توسط سلولهای دیوارهی معده افزایش یافته و باعث درد، التهاب و گاهی خونریزی معده میشود.
یکی از راههای درمان و کاهش درد معده، استفاده از ضداسیدها است که توسط پزشکان تجویز میشود. همانطور که اسم ضداسیدها دارده داد میزنه! این مواد خاصیت بازی دارند و میتوانند با اسید معده واکنش داده و آنرا خنثی کنند.
* شیر منیزی یکی از رایجترین ضداسیدهاست که شامل منیزیم هیدروکسید است. این دارو مطابق معادلهی زیر با اسید معده واکنش میدهد و باعث کاهش اسید معده میشود.
$2HCl(aq)+Mg{{(OH)}_{2}}(s)\to MgC{{l}_{2}}(aq)+2{{H}_{2}}O(l)$