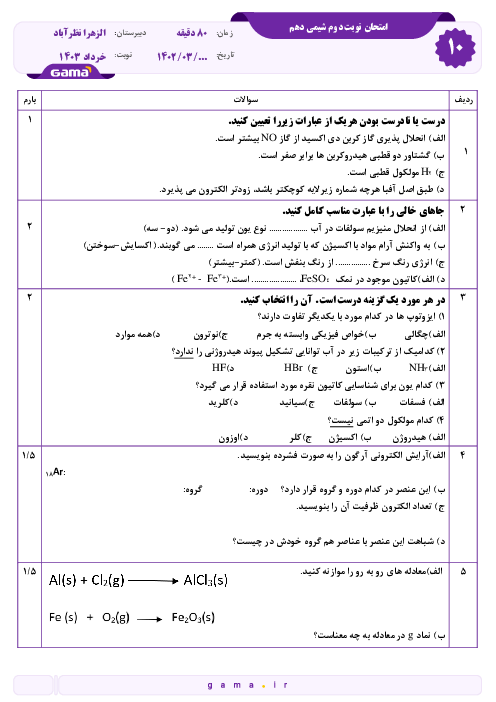
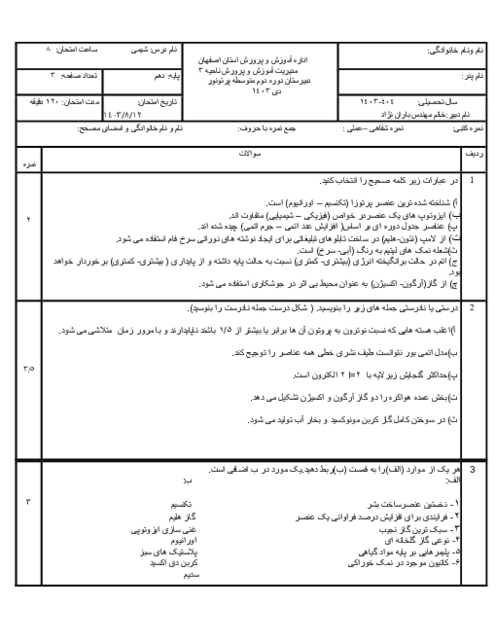
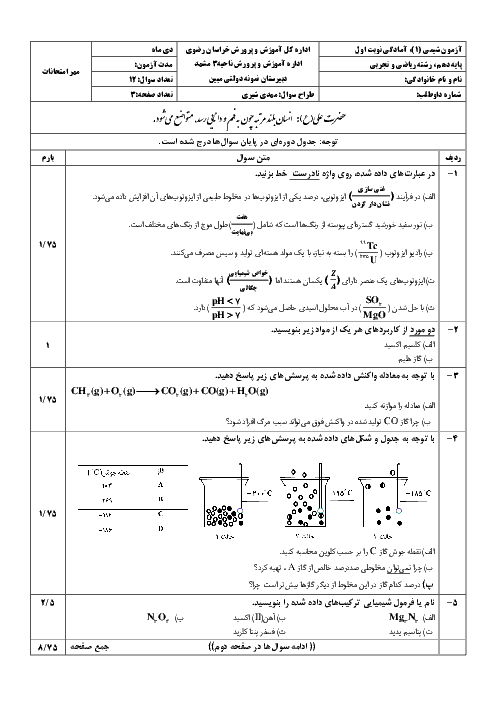
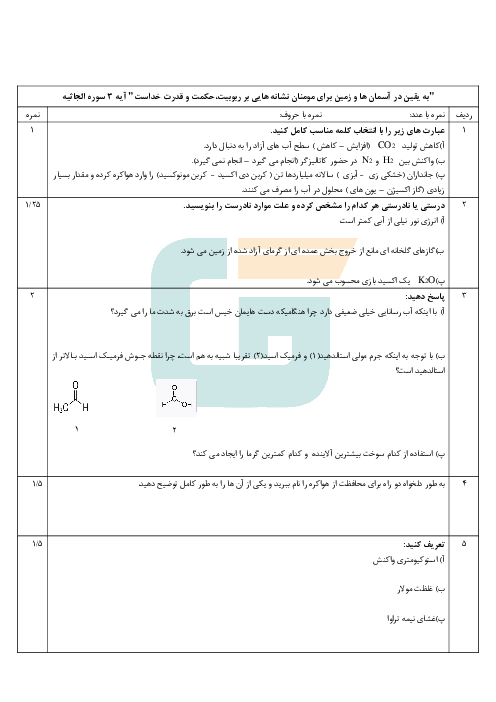عنصر X دارای 3 ایزوتوپ است که درصد فراوانی سبکترین و سنگینترین ایزوتوپ آن به ترتیب 50% و 20% است. سنگینترین ایزوتوپ 2 نوترون بیشتر از سبکترین ایزوتوپ و 1 نوترون بیشتر از ایزوتوپ دیگر دارد و جرم اتمی میانگین این عنصر 36.7 میباشد. اگر در کاتیون ${X^{2 + }}$ سبکترین ایزوتوپ اختلاف نوترون و الکترون 6 واحد باشد، این عنصر به ترتیب در کدام گروه است و چند الکترون با l=1 دارد؟
تحلیل ویدئویی تست
منتظریم اولین نفر تحلیلش کنه!