اگر واکنش $V(s)+F{{e}^{2+}}(aq)\to {{V}^{2+}}(aq)+Fe(s)$ انجام پذیر باشد، ولی واکنش $+F{{e}^{2+}}(aq)+Ni(s)\to Fe(s)+N{{i}^{2+}}(aq)$ انجام ناپذیر باشد، کدام گزینه در رابطه با آنها صحیح است؟
1 )
قدرت الکترون دادن $Ni$ بیشتر از $V$ است.
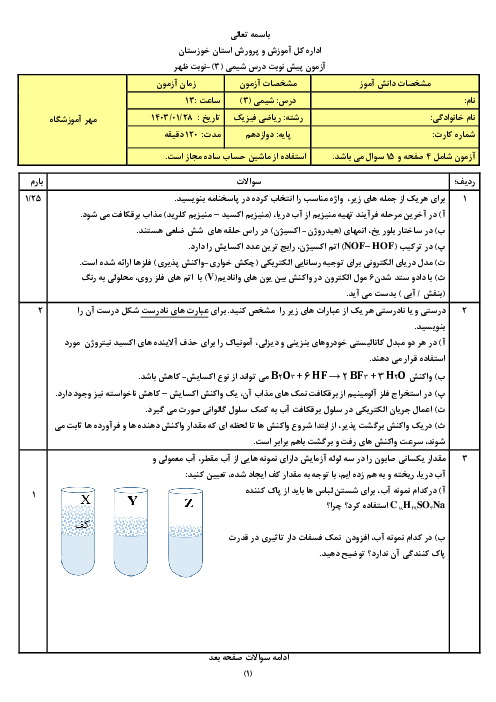
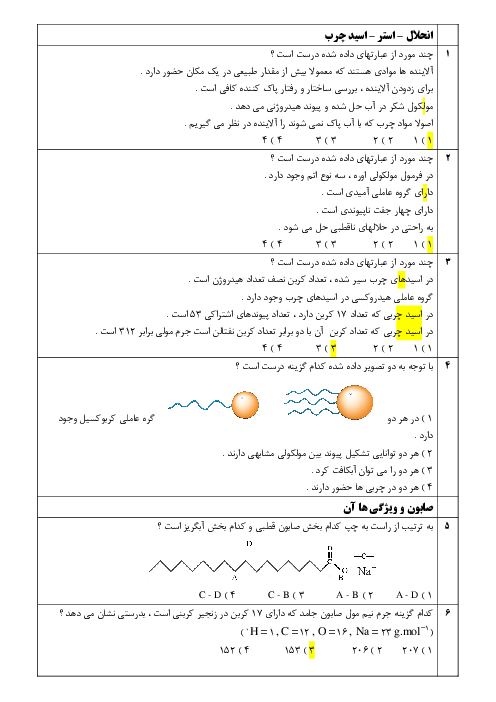
2 )
ضمن انجام واکنش اول، کاتیون ${{Fe}^{2+}}$ از نیم سلول آند به سمت کاتد حرکت میکند.
در واكنش اول با گذشت زمان، جرم تيغهٔ كاتد همانند غلظت ${{V}^{2+}}$ زیاد میشود.
4 )
فلز نیکل میتواند یون ${{V}^{2+}}$ را از حالت محلول خارج کند.