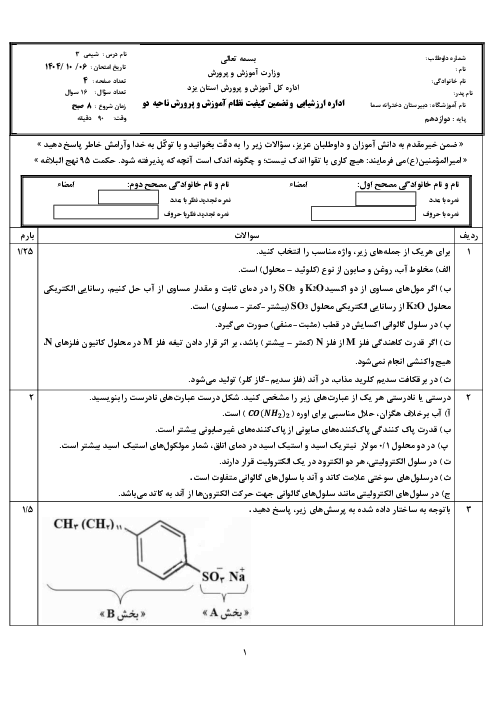
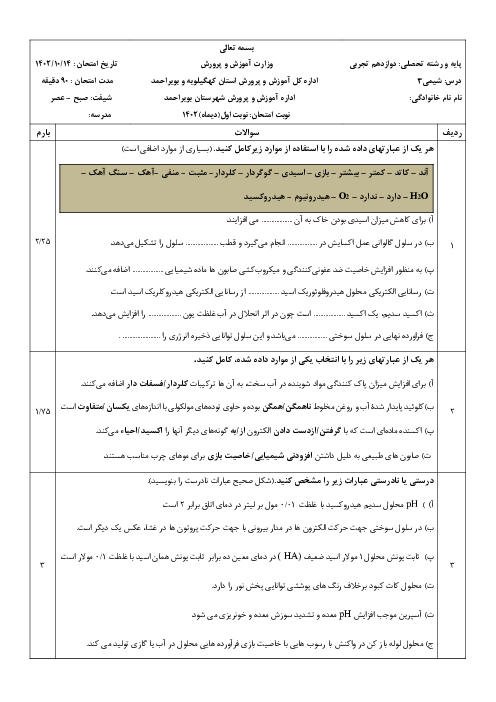
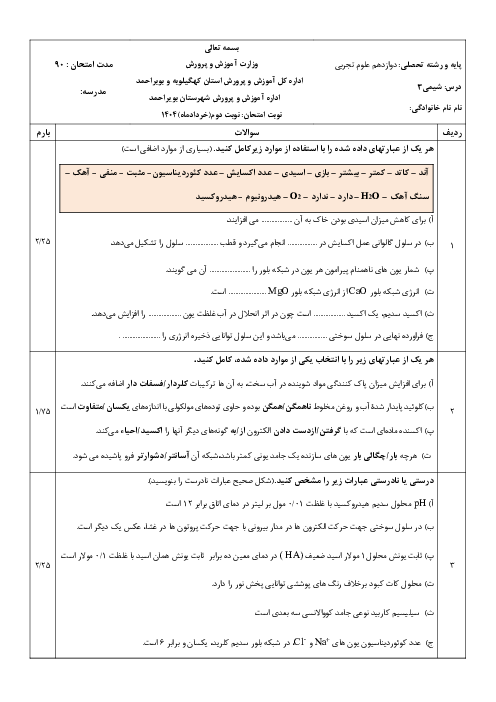
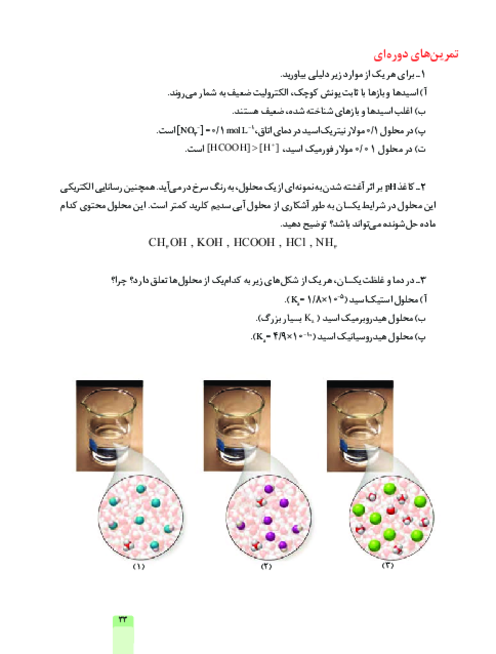
مطابق واكنش زير، از حل كردن ${{N}_{2}}{{O}_{5}}$ در آب $HN{{O}_{3}}$ تولید میشود.
${{N}_{2}}{{O}_{5}}+{{H}_{2}}O\to 2HN{{O}_{3}}$
$?molHN{{O}_{3}}=2/8L{{N}_{2}}{{O}_{5}}\times \frac{1mol{{N}_{2}}{{O}_{5}}}{22/4L{{N}_{2}}{{O}_{5}}}\times \frac{2molHN{{O}_{3}}}{1mol{{N}_{2}}{{O}_{5}}}=\frac{1}{4}molHN{{O}_{3}}$
از آنجایی که از انحلال $N{{a}_{2}}O$ در آب، $NaOH$ بهدست میآید، پس باید اسید $HN{{O}_{3}}$ و باز $NaOH$ یکدیگر را خنثی کنند.
$NaOH+HN{{O}_{3}}\to NaN{{O}_{3}}+{{H}_{2}}O$
$?molNaOH=\frac{1}{4}molHN{{O}_{3}}\times \frac{1molNaOH}{1molHN{{O}_{3}}}=\frac{1}{4}molNaOH$
حال طبق واکنش زیر باید مقدار گرم $N{{a}_{2}}O$ اولیه را به ازای تولید $\frac{1}{4}$ مول $NaOH$ بهدست آوریم.
$N{{a}_{2}}O+{{H}_{2}}O\to 2NaOH$
$?gN{{a}_{2}}O=\frac{1}{4}molNaOH\times \frac{1molN{{a}_{2}}O}{2molNaOH}\times \frac{62gN{{a}_{2}}O}{1molN{{a}_{2}}O}=7/75gN{{a}_{2}}O$