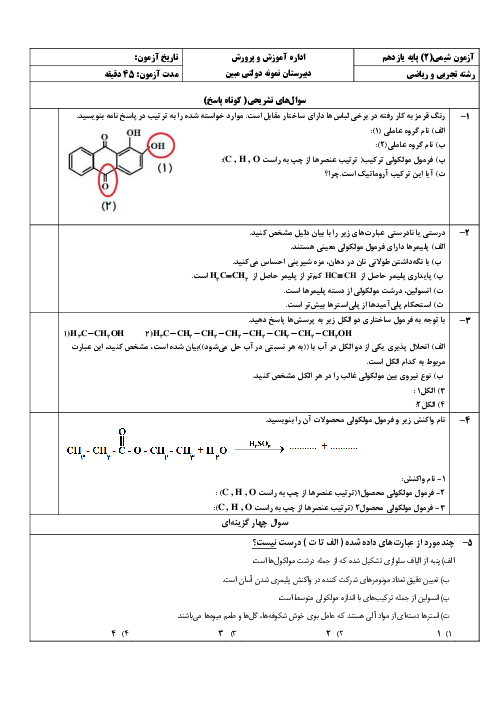
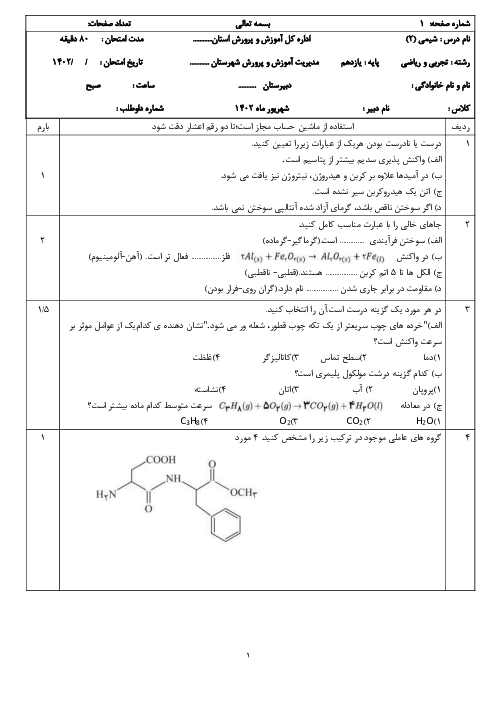
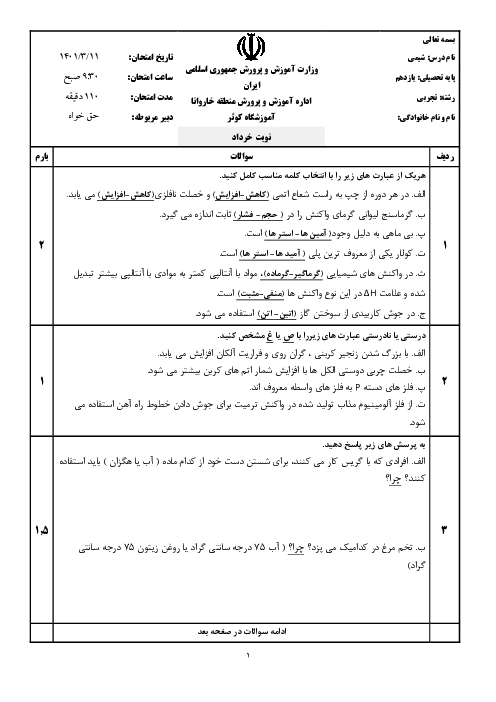
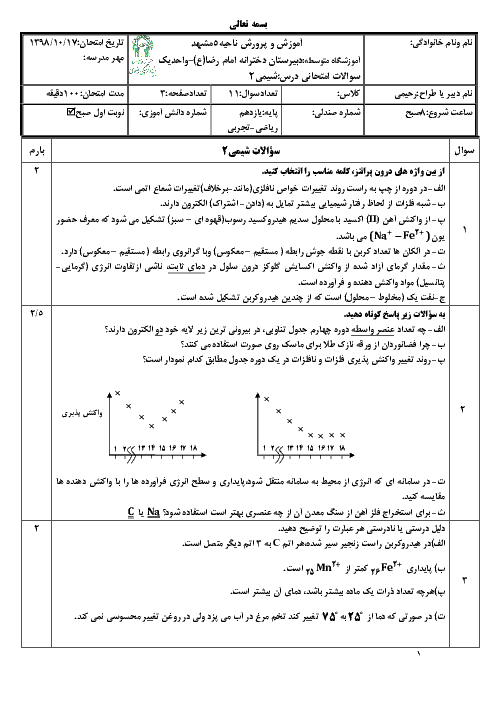
اگر هر کیلوگرم از یک نمونه آب دارای 1/164 گرم یون هیدروژن سولفات باشد، برای خنثی کردن این یون در یک تن از این نمونه آب، چند گرم سدیم هیدروکسید مصرف میشود، در صورتی که بازده درصدی واکنش برابر 80 درصد باشد؟
$(H=1g.mo{{l}^{-1}},Na=23g.mo{{l}^{-1}},O=16g.mo{{l}^{-1}},S=32g.mo{{l}^{-1}})$
$HSO_{4}^{-}+NaOH\to NaSO_{4}^{-}+{{H}_{2}}O$
1 )
500
2 )
1000
600
4 )
1200
تحلیل ویدئویی تست
منتظریم اولین نفر تحلیلش کنه!