بررسی گزینهها:
گزینۀ «1» : نادرست. در برقکافت آب که در یک سلول الکترولیتی صورت میگیرد، در اطراف آند (قطب مثبت) نیم واکنش اکسایش به صورت زیر رخ میدهد و ضمن تولید ${{H}^{+}}$ محیط اسیدی میشود.
$2{{H}_{2}}O(l)\to {{O}_{2}}(g)+4{{H}^{+}}(aq)+4{{e}^{-}}$
گزینۀ «2» : نادرست. ${{E}^{0}}$ نیم واکنش کاتدی (کاهش) در فرایند خوردگی در دو محیط اسیدی و غیر اسیدی به صورت زیر است:
محیط اسیدی ${{O}_{2}}(g)+4{{H}^{+}}(aq)+4{{e}^{-}}\to 2{{H}_{2}}O(l){{E}^{0}}=+1/23V$
محیط غیر اسیدی ${{O}_{2}}(g)+2{{H}_{2}}O(l)+4{{e}^{-}}\to 4O{{H}^{-}}(aq){{E}^{0}}=+0/40V$
با توجه به بیشتر بودن (کاتد) ${{E}^{0}}$ در محیط اسیدی، خوردگی آهن در این محیط با سرعت بیشتری رخ میدهد. (emf سلول بزرگتر میشود.)
گزینۀ «3» : درست. در اثر ایجاد خراش در حلبی یا آهن سفید و یا فرایند خوردگی، نیمواکنش کاهش به صورت زیر است که در آن اکسیژن الکترون دریافت کرده و کاهش مییابد.
${{O}_{2}}(g)+2{{H}_{2}}O(l)+4{{e}^{-}}\to 4O{{H}^{-}}(aq)$
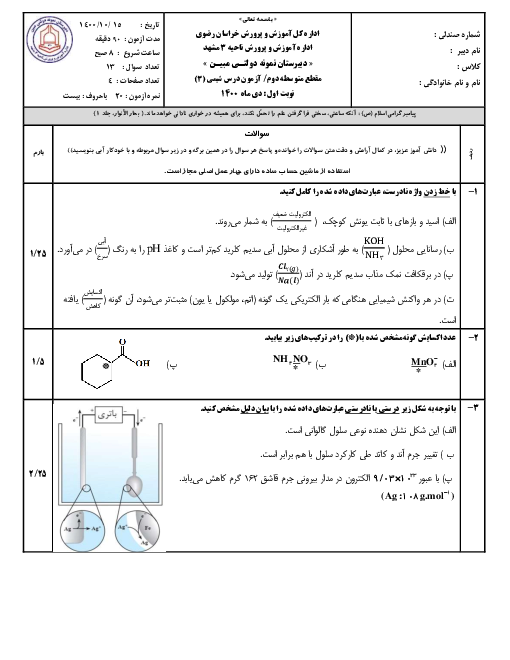
گزینۀ «4» : نادرست. در فرایند آبکاری فلز پوشاننده به قطب مثبت (آند) متصل است و دچار اکسایش میشود. اما نیم واکنش کاهش نیز مربوط به فلز پوشاننده آن میشود. به عنوان مثال نیم واکنشهای اکسایش و کاهش در فرایند آبکاری با فلز نقره به صورت زیر است:
نیم واکنش اکسایش $Ag(s)\to A{{g}^{+}}(aq)+{{e}^{-}}$
نیم واکنش کاهش $A{{g}^{+}}(aq)+{{e}^{-}}\to Ag(s)$