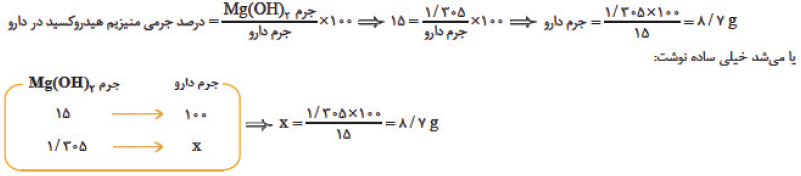در بدن انسان بالغ، روزانه $3$ لیتر شیرهی معده تولید میشود، اگر غلظت منیزیم هیدروکسید در یک نمونه داروی ضداسید معده $15$ درصد جرمی باشد، برای خنثی کردن نیمی از اسید معده، روزانه به جند گرم از این دارو نیاز است؟ $(Mg=24,O=16,H=1:g.mo{{l}^{-1}})$
تحلیل ویدئویی تست
منتظریم اولین نفر تحلیلش کنه!