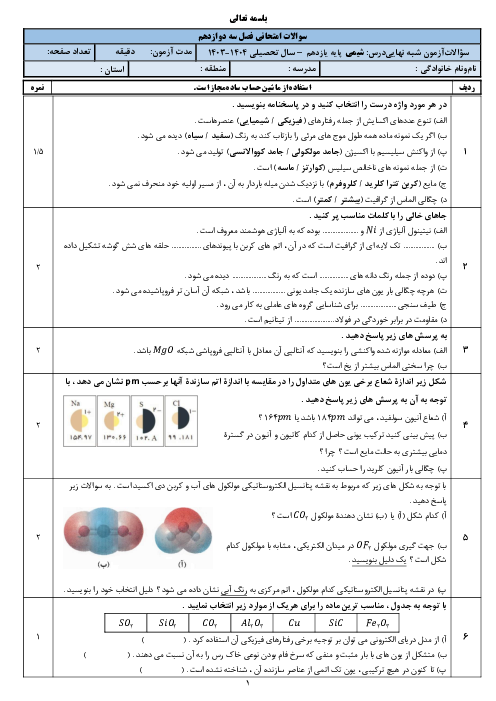
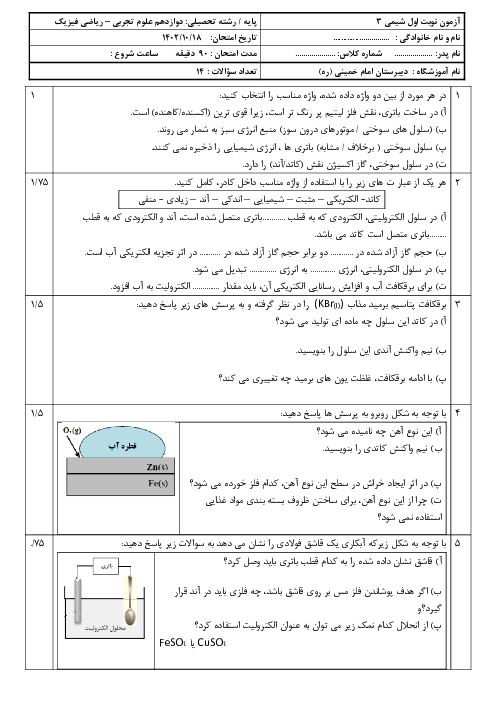
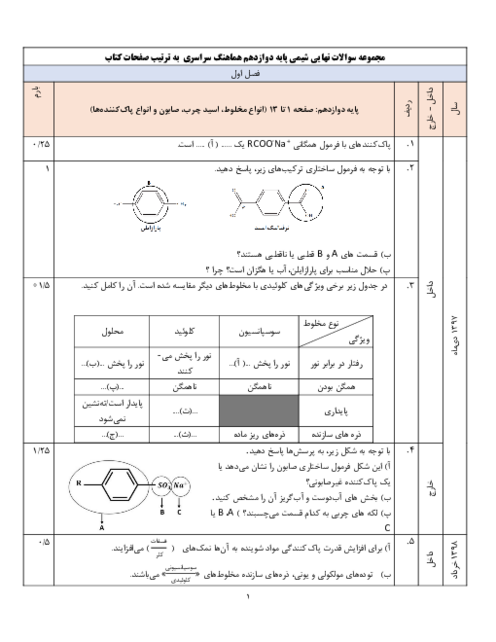
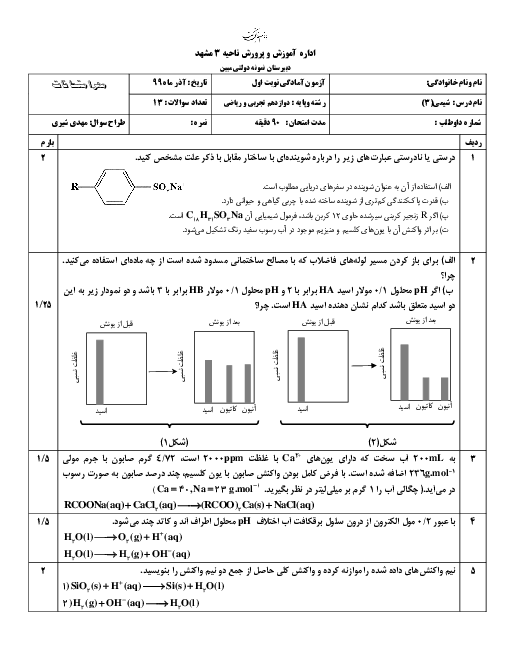
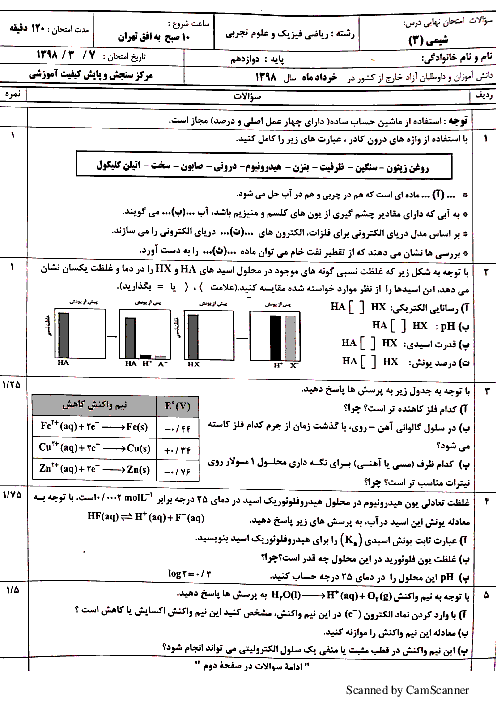
ثابت یونش اسیدها تنها به دما وابسته است و با تغییر مقدار اولیه واکنشدهندهها تغییر نمیکند. ثابت یونش، بیانی از میزان پیشرفت فرایند یونش تا رسیدن به تعادل است. هرچه ثابت یونش بزرگتر باشد، اسید قویتر است. در محلول اسیدهای ضعیف که 𝐾 𝑎 K a کوچکی دارند، غلظت تعادلی اسید از غلظت تعادلی هر یک از یونها بیشتر است. در محلول اسیدهای قوی که 𝐾 𝑎 K a بزرگی دارند، غلظت تعادلی اسید از غلظت تعادلی هر یک از یونها کمتر است. اسید قویتر با 𝐾 𝑎 K a بزرگتر، در غلظت یکسان، غلظت یون هیدرونیوم در محلول آن بیشتر است. سرعت واکنش فلزات با محلولهای اسید بستگی به غلظت یون هیدرونیوم دارد. هرچه اسید قویتر باشد، سرعت واکنش بیشتر است.
نکات مهم درباره ثابت یونش اسیدها چیست؟
پاسخ ها: {{ repliesNum }}
پاسخ انتخاب شده
در پاسخ به: {{ reply.reply_to.name }}
در پاسخ به
این پیام حذف شده است.