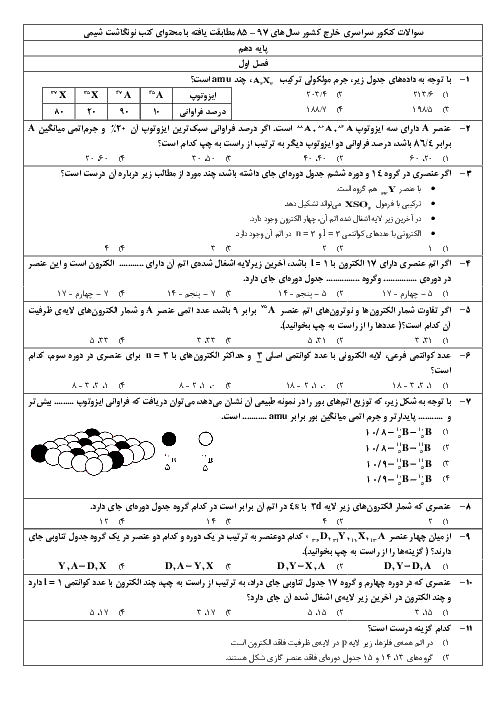
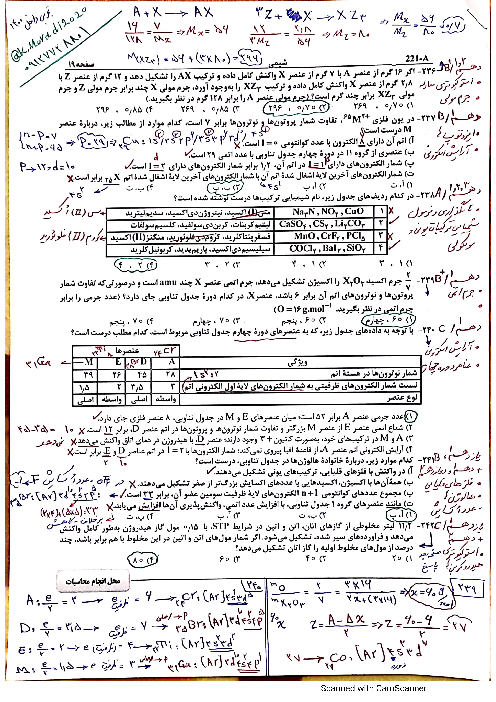
سلام دربارهی عبارت( جرم 120 عدد از اتم های فراوان ترین ایزوتوپ هیدروژن در مقایسه با جرم 10 اتم C¹²(شش پروتون و شش نوترون) بیشتر است) ؛ پاسخ نامه بیان کرده به دلیل اینکه هر H 1/008 amu هست و 120×1/008 > 120×1 پس این عبارت صحیح است. اما دلیل من اینه که هر H یک پروتون( یعنی کلا 120 پروتون) اما در هر C شش پروتون و شش نوترون داریم ( کلا 60 پروتون و 60 نوترون) داریم و با توجه به اینکه جرم یک نوترون از جرم یک پروتون بیشتره پس این جمله اشتباه و جرم بیان شده در قسمت دوم عبارت بیشتره. کدام تحلیل درست هست؟
آیا جرم 120 عدد از اتمهای فراوانترین ایزوتوپ هیدروژن در مقایسه با جرم 10 اتم C¹² (شش پروتون و شش نوترون) بیشتر است؟
پاسخ ها: {{ repliesNum }}
پاسخ انتخاب شده
در پاسخ به: {{ reply.reply_to.name }}
در پاسخ به
این پیام حذف شده است.