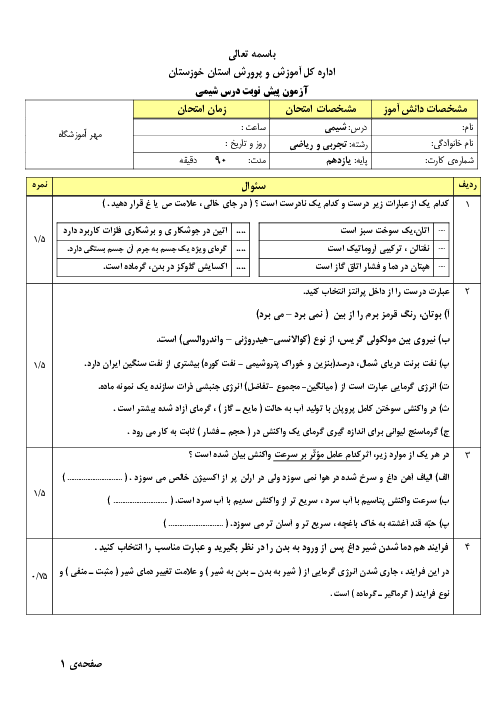
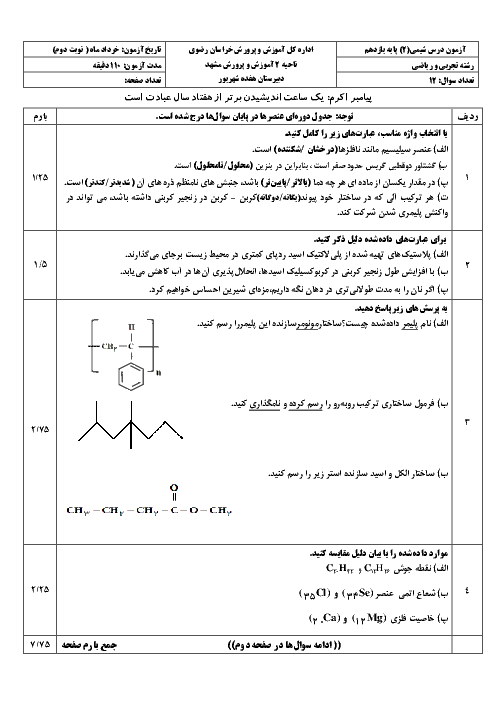
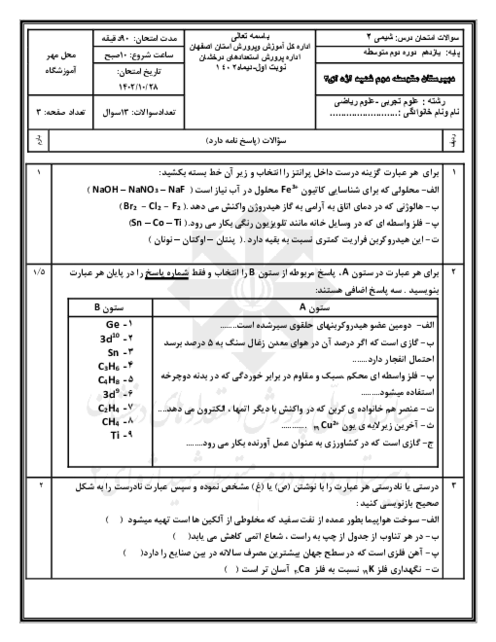
از واکنش 380 گرم Ticl4 مقدار 75 گرم تیتانیوم به دست امده است . مقدار نظری و بازده درصدی آن را محاسبه کنید؟ Ticl4(g) +2mg(s) --->Ti (s) + 2mgcl2(i) Ti=48 Ticl4=190
از واکنش 380 گرم Ticl4 مقدار 75 گرم تیتانیوم به دست آمده است. مقدار نظری و بازده درصدی آن را محاسبه کنید.
پاسخ ها: {{ repliesNum }}
پاسخ انتخاب شده
در پاسخ به: {{ reply.reply_to.name }}
در پاسخ به
این پیام حذف شده است.