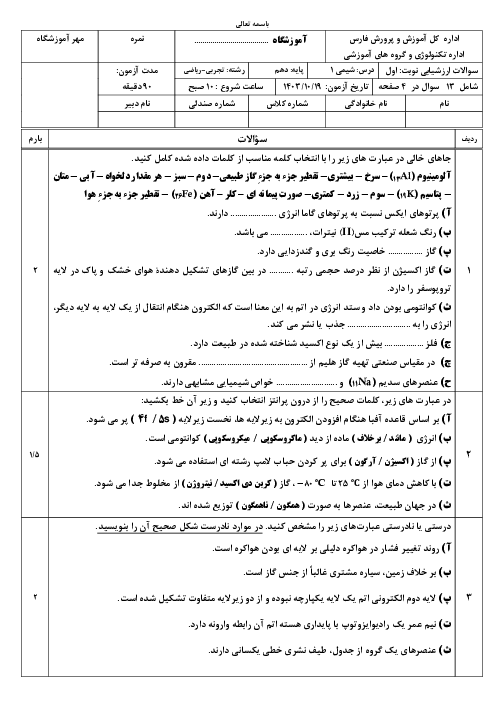
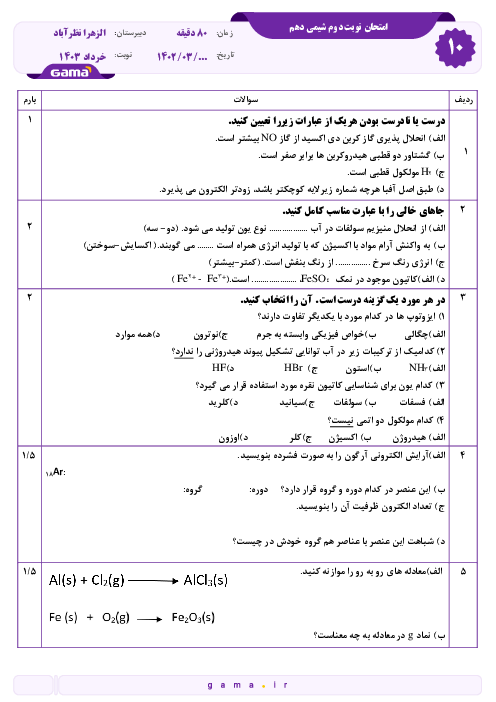
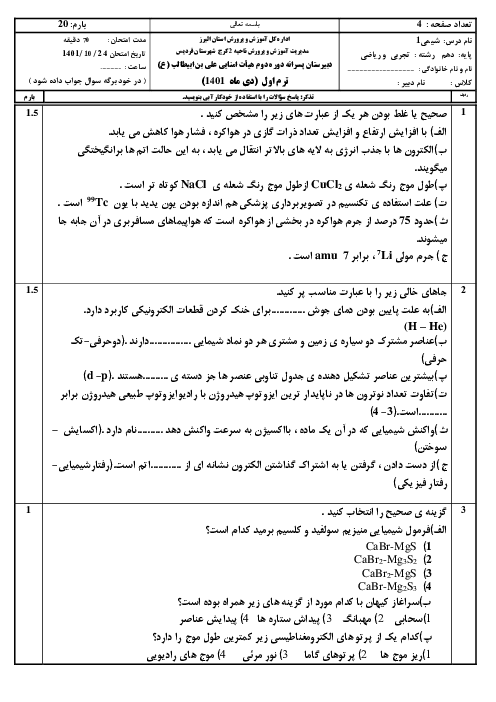
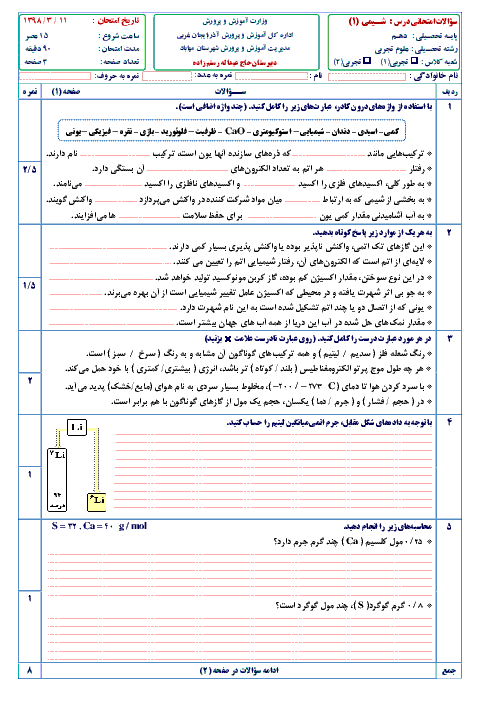
طبق واکنش زیر, 4.5 گرم فلز آلومینیوم را در چند میلی لیتر محلول سولفوریک اسید 49 درصد جرمی با چگالی 1.2 g/mL اضافه کنیم تا واکنش به طور کامل انجام شود. Al(s) + H2SO4(aq) => Al(SO4)3(aq) + H2(g) (واکنش موازنه شود) (32=H=1 O=16 Al=27 S) g.mol
با توجه به واکنش زیر حجم سولفوریک اسید را محاسبه کنید.
پاسخ ها: {{ repliesNum }}
پاسخ انتخاب شده
در پاسخ به: {{ reply.reply_to.name }}
در پاسخ به
این پیام حذف شده است.