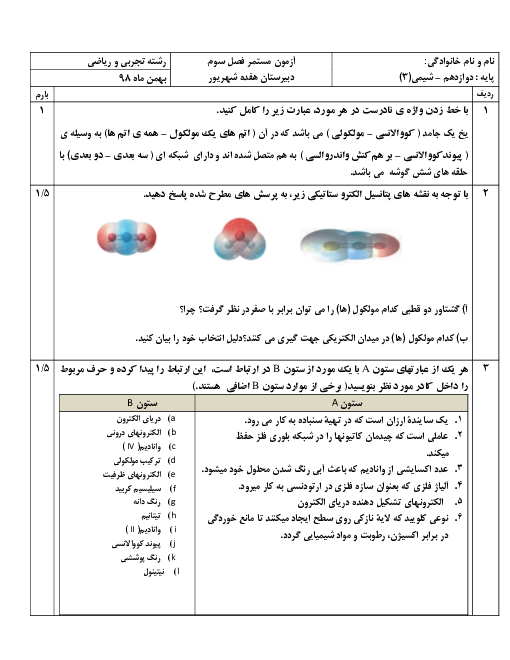
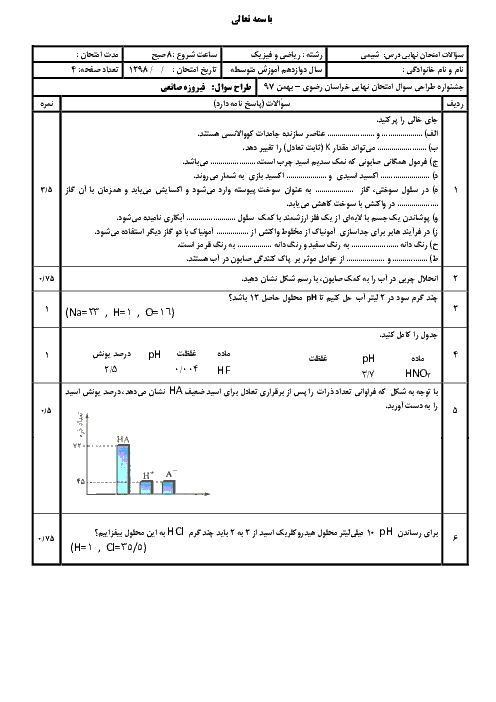
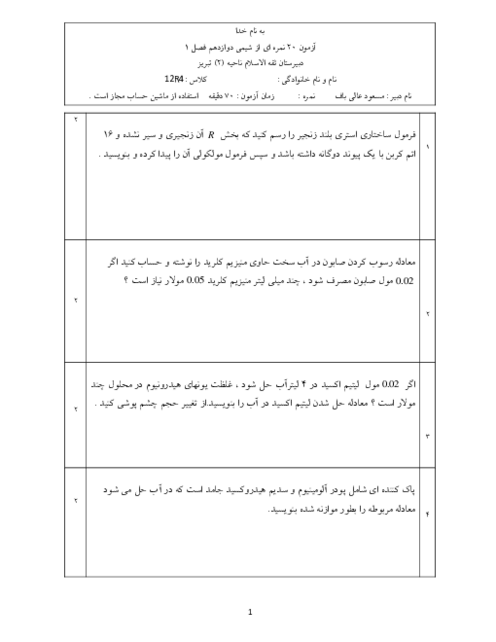
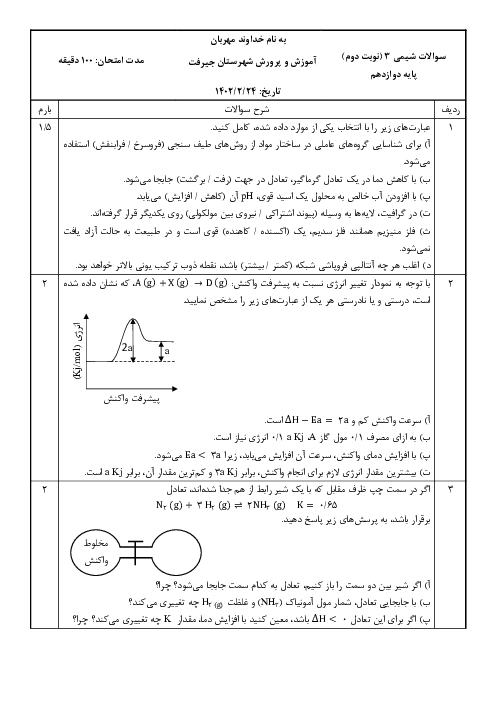
HAیک اسید ضعیف است.این اسید به طور جزیی در اب به +H و -A یو نیده می شود . وقتی 1 مول HA در مقدار مناسبی اب حل شود:مجموع مولکول های HA یونیده نشده و یون های +H و -A در محلول روی هم برابر 1/1 مول می شود . در صد یونیده شدن مولکول های HAدر شرایط داده شده چند است؟
درصد یونش مولکول های یک اسید ضعیف در آب
پاسخ ها: {{ repliesNum }}
پاسخ انتخاب شده
در پاسخ به: {{ reply.reply_to.name }}
در پاسخ به
این پیام حذف شده است.