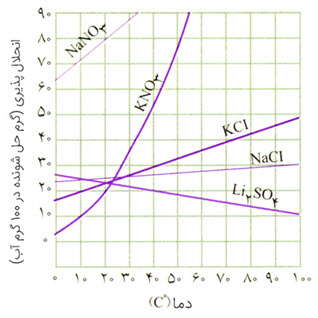
با توجه به نمودار، محلول سیر شدهای از $KCl$ در 300 گرم آب در دمای $60{}^\circ C$ تهیه شده است. در کدام دما (${}^\circ C$) غلظت این محلول 4 مولار بوده و در این دما چند گرم از این نمک رسوب میکند؟ (از تغییر حجم چشم پوشی شود و چگالی آن برابر $1g.mL^{-1}$است) ($KCl=74/5g.mol^{-1}$)
تحلیل ویدئویی تست
منتظریم اولین نفر تحلیلش کنه!