در واکنشهای اول و چهارم عدد اکسایش هیچ عنصری تغییر نکرده است، پس از نوع اکسایش ـ کاهش نیستند.
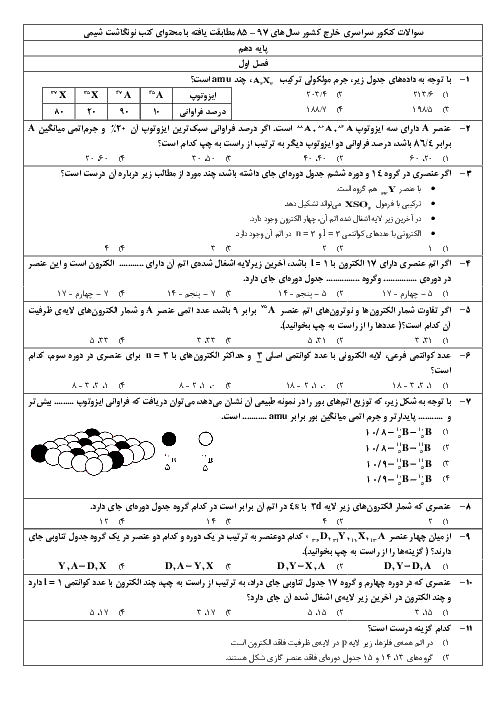
برای موازنهٔ دو واکنش دیگر از روش اکسایش ـ کاهش استفاده میکنیم، به این صورت که تغییر عدد اکسایش کاهنده را ضریب اکسنده و تغییر عدد اکسایش اکسنده را ضریب کاهنده قرار میدهیم.
عدد اکسایش ید از صفر در ${I_2}$ به 5+ در $IO_3^ - $ رسیده است؛ با توجه به اینکه در سمت چپ معادله، دو اتم ید داریم، تغییر عدد اکسایش آن را در 2 ضرب میکنیم میشه 10. عدد اکسایش $Cl$ از 5+ در $ClO_3^ - $ به 1- در $C{l^ - }$ رسیده، یعنی 6 واحد تغییر کرده است.
اعداد 6 و 10 را اگر ساده کنیم، میرسیم به 3 و 5! 5 را ضریب $ClO_3^ - $ و 3 را ضریب ${I_2}$ قرار میدهیم:
$\underline 3 {I_2}\underline 5 ClO_3^ - + - {H_2}O \to - IO_3^ - + - {H^ + } + - C{l^ - }$
به این ترتیب باید ضریب $IO_3^ - $ برابر 6 و ضریب $C{l^ - }$ برابر با 5 باشد. برای موازنهٔ بار هم ضریب ${H^ + }$ باید 6 و در نتیجه ضریب ${H_2}O$ باید 3 باشد:
$3{I_2} + 5ClO_3^ - + 3{H_2}O \to 6IO_3^ - + 6{H^ + } + 5C{l^ - }$
مجموع ضرایب گونهها در این واکنش برابر با 28 است.
اگر همین مراحل را برای واکنش سوم انجام بدین، متوجه خواهید شد که ضرایب همهٔ گونهها در معادلهٔ موازنهشده این واکنش برابر با یک است.
$Pb(OH)_3^ - + Cl{O^ - } \to Pb{O_2} + C{l^ - } + O{H^ - } + {H_2}O$
یعنی مجموع ضرایب همهٔ گونهها در آن برابر با 6 است:
$28 - 6 = 22$