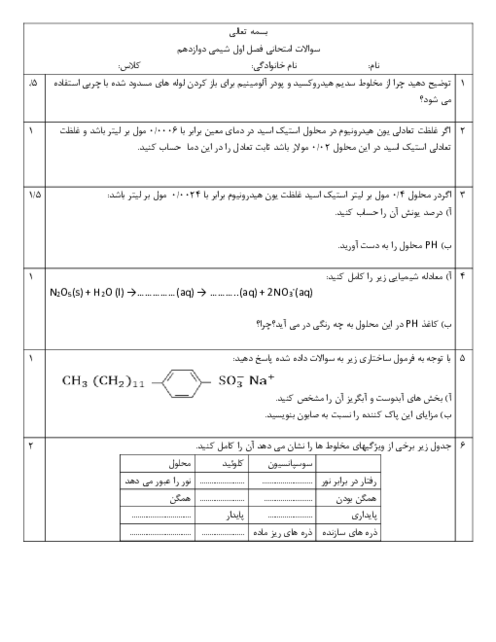
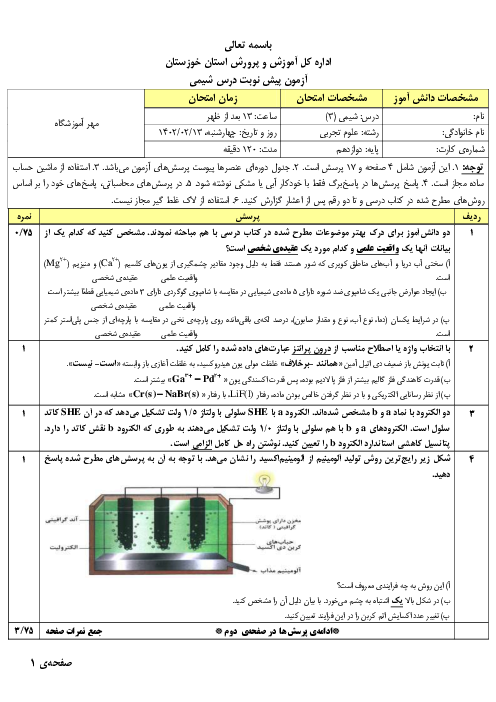
تمام گزينهها درباره فرايند برقكافت آب صحيح است، بهجز: $(H=1,O=16:g.mo{{l}^{-1}})$
1 )
گاز توليد شده در كاتد را میتوان برای نيم واكنش آندی در سلول سوختی استفاده كرد.
2 )
گاز اكسيژن در اطراف الكترودی توليد میشود كه به قطب مثبت باتری متصل شده است.
3 )
با گذشت زمان $pH$ آب، خنثی باقی میماند.
به ازای تولید $4$ گرم گاز در آند $2mol$ الکترون تولید میشود.