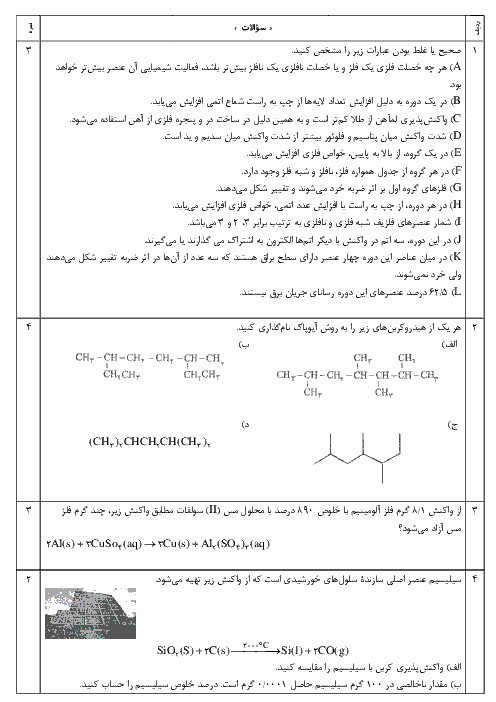
ابتدا انرژی لازم برای تبدیل 1 مول بخار آب به اتمهای سازنده گازی را محاسبه میكنیم. سپس مولهای حاصل از سوزاندن 60 گرم گلوكز را بدست میآوریم:
${{H}_{2}}O(g)\to O(g)+2H(g)$
$\Delta H=2\Delta H(O-H)=2\times 463=926kJ.mo{{l}^{-1}}$
${{C}_{6}}{{H}_{12}}{{O}_{6}}(s)+6{{O}_{2}}(g)\to 6C{{O}_{2}}(g)+6{{H}_{2}}O(g)$
$?mol\,{{H}_{2}}O=60g\,{{C}_{6}}{{H}_{12}}{{O}_{6}}\times \frac{1mol\,{{C}_{6}}{{H}_{12}}{{O}_{6}}}{180g\,{{C}_{6}}{{H}_{12}}{{O}_{6}}}$
$\times \frac{6mol\,{{H}_{2}}O}{1mol\,{{C}_{6}}{{H}_{12}}{{O}_{6}}}=2mol\,{{H}_{2}}O$
$?kJ=2mol\,{{H}_{2}}O\times \frac{926kJ}{1mol\,{{H}_{2}}O}=1852kJ$