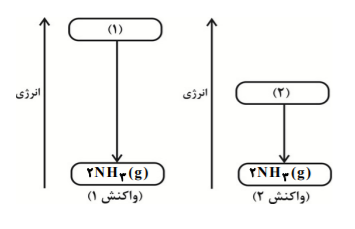
با توجه به نمودارهای انرژی زیر كدام گزینه نادرست است؟ (واكنش (1) در دمای $({{20}^{\circ }}C)$ و واكنش (2) در دمای $({{25}^{\circ }}C)$ انجام میشود.)
1 )
علامت آنتالپی هر دو واكنش منفی است.
2 )
اگر مواد واكنش دهنده در واكنش (2) شامل${{N}_{2}}(g)$ و ${{H}_{2}}(g)$ باشد، مواد واکنش دهنده در واکنش (1) میتواند شامل ${{N}_{2}}{{H}_{4}}(g)$ و ${{H}_{2}}(g)$ باشد.
3 )
واكنشدهندهها در واكنش (2) پایداری بیشتری از واكنشدهندهها در واكنش (1) دارند.
تفاوت آنتالپی در دو واكنش تنها به دلیل انجام آنها در شرایط دمایی متفاوت است.