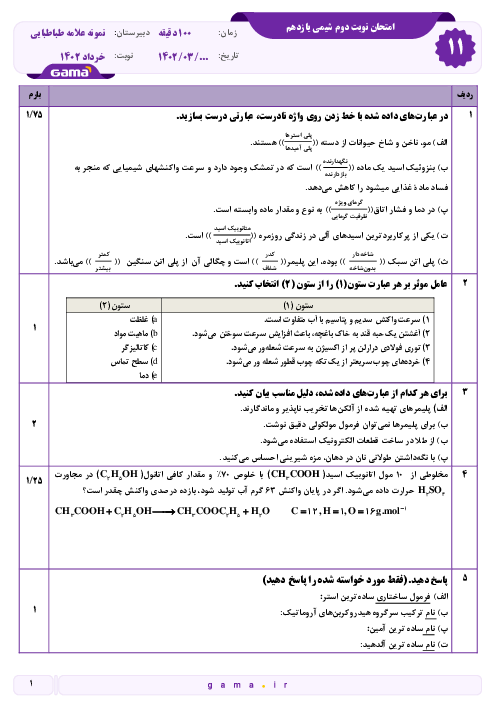
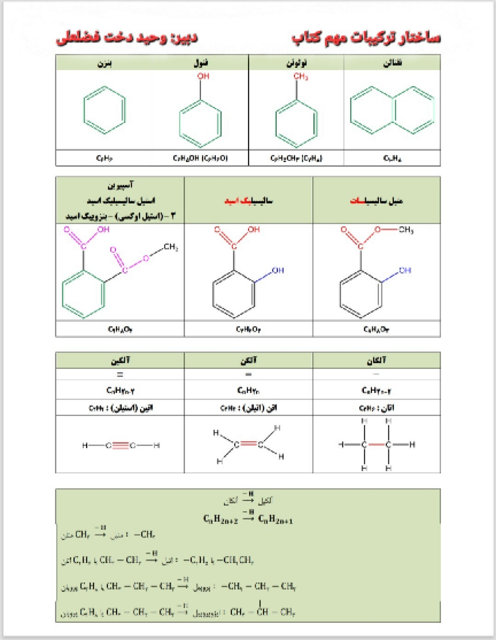
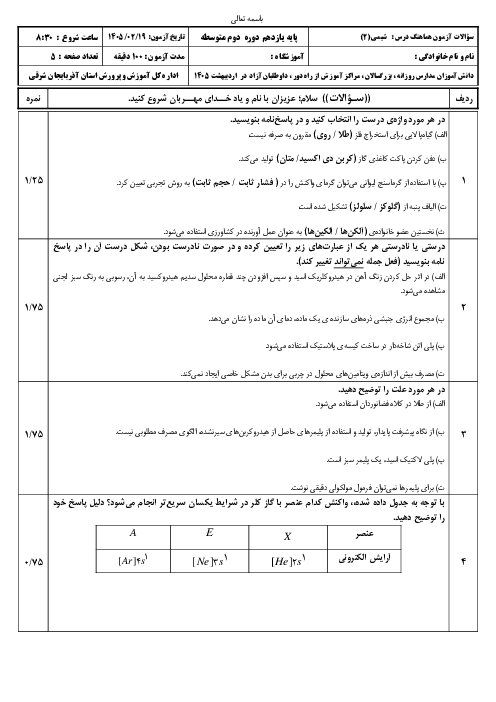
قسمت 6: دنیای واقعی واکنشها (استوکیومتری)
شیمی (2)
یازدهم
متوسطه دوم نظری
علوم تجربی
درسنامه آموزشی این مبحث
اگر در واکنش (موازنه نشده): $L{{i}_{3}}N(s)+{{H}_{2}}O(l)\to LiOH(aq)+N{{H}_{3}}(aq)$، 0/5 مول لیتیم نیترید مصرف شود و بازده درصدی واکنش 80 درصد باشد، فرآوردههای واکنش در مجموع با چند مول HCl واکنش کامل میدهند؟