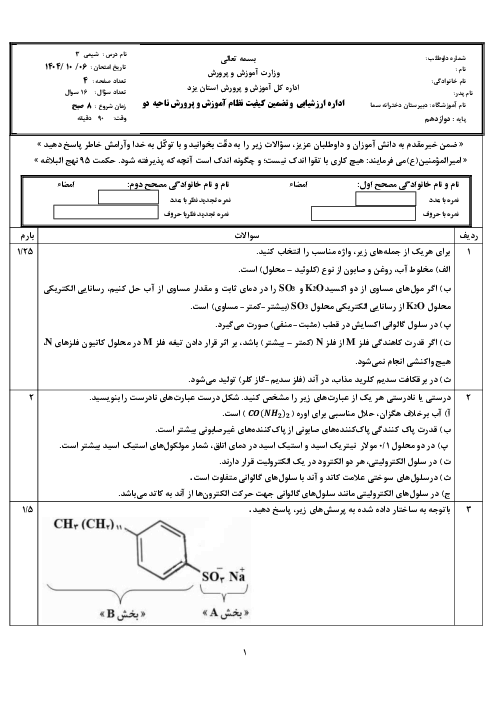
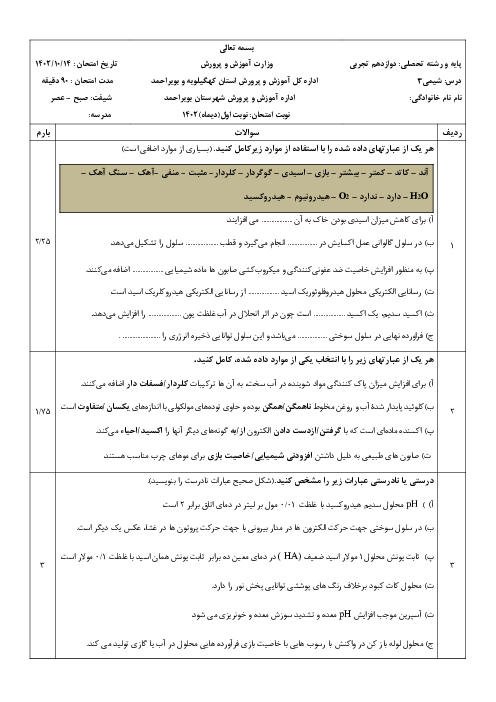
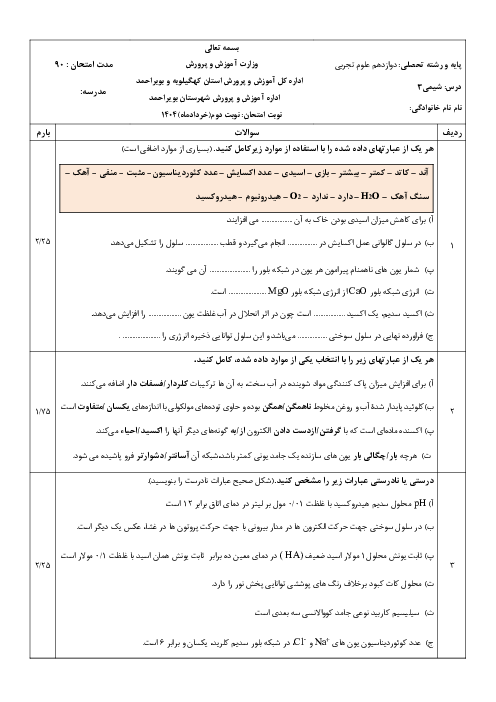
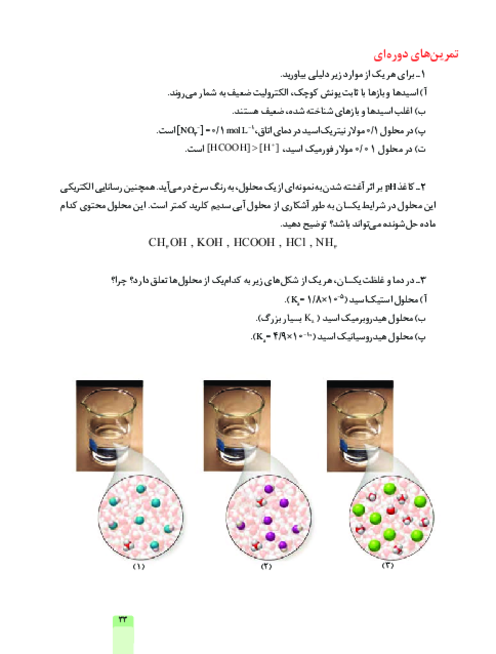
$2Al(s)+3C{{u}^{2+}}(aq)\to 2A{{l}^{3+}}(aq)+3Cu(s)$
محاسبهٔ مقدار مول $A{{l}^{3+}}$ تولید شده:
$?molA{{l}^{3+}}=36/12\times {{10}^{21}}e\times \frac{1mole}{6/02\times {{10}^{23}}e}\times \frac{2molA{{l}^{3+}}}{6mole}=0/02molA{{l}^{3+}}$
$\Rightarrow \left[ A{{l}^{3+}} \right]=\frac{0/02}{0/4}=0/05mol.{{L}^{-1}}$
محاسبه مقدار مول $C{{u}^{2+}}$ مصرف شده:
مصرفی $C{{u}^{2+}}$ کل $=molC{{u}^{2+}}$ مول $-molC{{u}^{2+}}$ باقیمانده
$=0/08-0/03=0/05molC{{u}^{2+}}$
$\Rightarrow \left[ C{{u}^{2+}} \right]=\frac{0/05}{0/4}=0/125mol.{{L}^{-1}}$
$\frac{\left[ C{{u}^{2+}} \right]}{\left[ A{{l}^{3+}} \right]}=\frac{0/125}{0/05}=2/5$