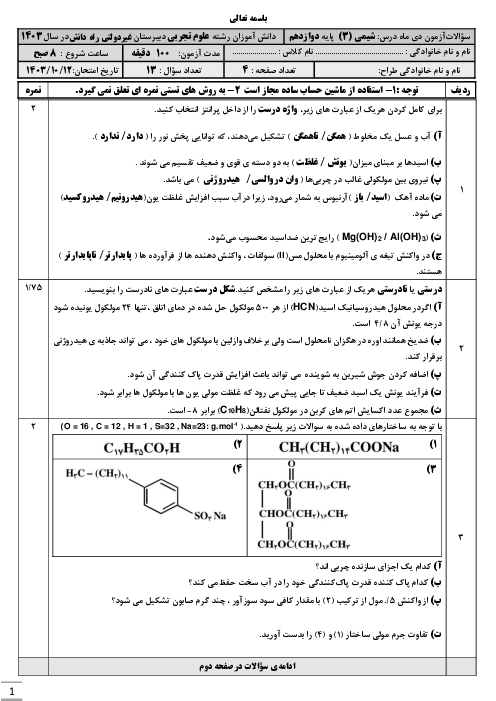
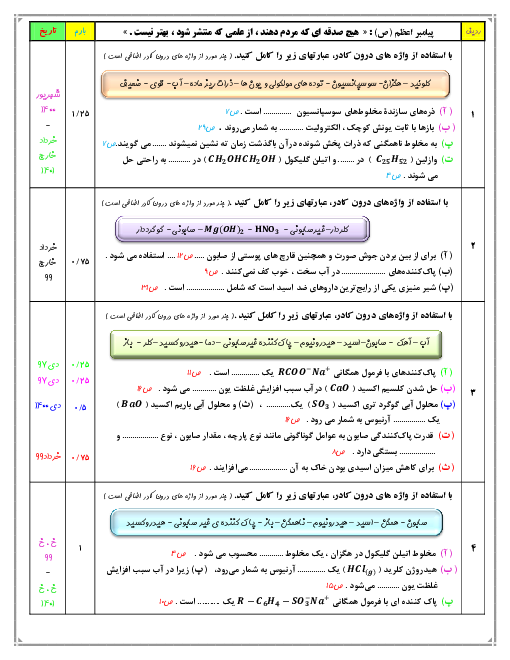
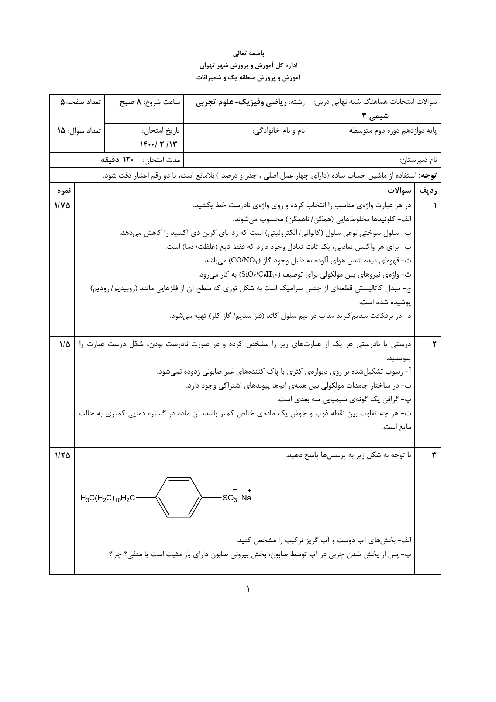
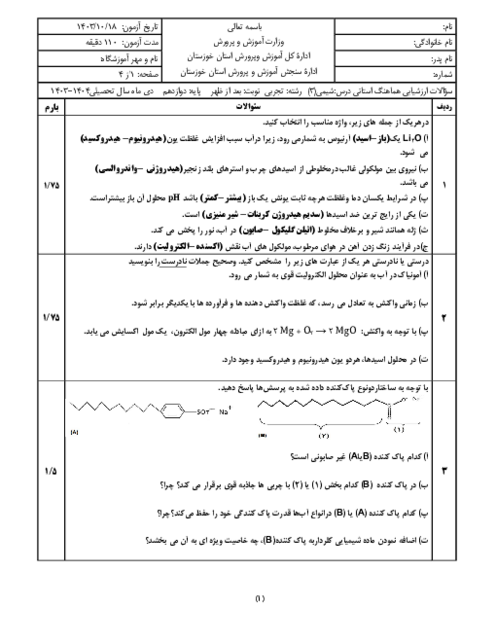
قسمت 4: سامانههای تعادلی و pH محلولها
شیمی (3)
دوازدهم
متوسطه دوم نظری
علوم ریاضی
درسنامه آموزشی این مبحث
$PH$ شيرهٔ معدهٔ فردی در حدود 2/7 است. برای خنثی نمودن ۵۰۰ ميلیليتر از اين محلول به چند ميلیليتر محلول منيزيم هيدروكسيد با $PH=13/3$ نیاز است؟ $\left( \log 2=0/3,\log 5=0/7 \right)$