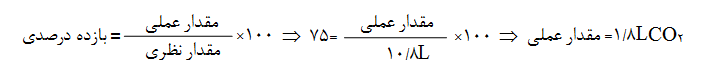مخلوطی از گازهای پروپان و اکسیژن در دمای ${{60}^{\circ }}C$ و فشار $21/6\,,\,1atm$ لیتر حجم را اشغال میکنند. اگر بر اثر جرقه با هم واکنش دهند و بهطور کامل مصرف شوند، حجم گازهای تولید شده در پایان واکنش در دمای ${{68}^{\circ }}C$ و فشار $1atm$، چند لیتر است؟ (بازده واکنش 75% است.)
تحلیل ویدئویی تست
منتظریم اولین نفر تحلیلش کنه!