اگر در واکنش تجزیهی دینیتروژن پنتوکسید، پس از گذشت $2$ دقیقه، افزایش حجم گازها با فرض شرایط $STP$، برابر $33/6$ لیتر باشد، سرعت متوسط مصرف واکنشدهنده چند مول بر دقیقه است؟
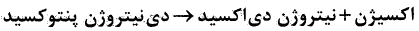
تحلیل ویدئویی تست
تحلیل ویدئویی برای این تست ثبت نشده است!

گاما رو نصب کن!
جستجو
پربازدیدها: #{{ tag.title }}
به پاس اعتمادی که به گاما داشتی، ما اشتراک ویژهای رو برات فعال کردیم تا بدون هیچ نگرانی از محدودیت زمانی، از سرویسهای ویژه گاما استفاده کنی.
اگه به اطلاعات بیشتری نیاز داری راهنمای تغییرات جدید رو ببین.
از همراهیت با گاما سپاسگزاریم.
با تقدیم احترام
با سپاس! گزارش شما ثبت شد.
اگر در واکنش تجزیهی دینیتروژن پنتوکسید، پس از گذشت $2$ دقیقه، افزایش حجم گازها با فرض شرایط $STP$، برابر $33/6$ لیتر باشد، سرعت متوسط مصرف واکنشدهنده چند مول بر دقیقه است؟
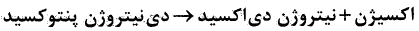
تحلیل ویدئویی برای این تست ثبت نشده است!